Coenzyme Q10 Ingredient Guide: CWS Powder vs. Liposomal CoQ10 for Superior Bioavailability
NavigatingCoQ10 Formulation Challenges: Solubility & Bioavailability
In the rapidly evolving health supplement market, Coenzyme Q10 (CoQ10) remains a cornerstone ingredient for cardiovascular health, anti-aging,とenergy metabolism。 However, for R&D managersと製品formulators, CoQ10 is notoriously difficult to work with.
As a naturally lipid-soluble crystalline powder, standard CoQ10 faces two significant "bottlenecks" that can hinder the commercial success of a finished product:
The Solubility Hurdle: Traditional CoQ10 has nearly zero solubility in water. This limits its application in the booming functional beverageとgummy sectors, where clarityとuniform dispersion are non-negotiable.
The Absorption Gap: Due to its large molecular weightとpoor water solubility, the native form of CoQ10 (Ubiquinone) exhibits low intestinal absorption. Ensuring that the active ingredient actually reaches the mitochondria—the "cellular powerhouse"—is a constant challenge for premium brand owners.
From "One-Size-Fits-All" to Precision Sourcing
At グリーン・春技術, we believe that the scientific properties of raw materials must translate into tangible product efficacy. Understanding these physiological barriers is the first step in selecting the right ingredient grade.
Whether you are formulating a standard softgel or a next-generation liposomal serum, choosing a supplier who understands the intersection of material science and biological efficacy is crucial for maintaining market competitiveness.
Selecting the Optimal CoQ10 Grade for Your Product Line
Not all Coenzyme Q10 ingredients are created equal. The choice of raw material directly impacts the stability, shelf-life, and consumer-perceived efficacy of the final product. Based on our 20 years of industry expertise, we have categorized CoQ10 grades into three primary technology pathways to meet diverse formulation needs.
Technical 仕様 & Application Matrix
To simplify your sourcing process, we have summarized our core CoQ10 offerings in the table below:
| Ingredient Grade | Specification | Key Features | Target Application |
| Standard CoQ10 (Ubiquinone) | ≥98% Purity (USP/EP) | High purity, Cost-effective, Lipid-soluble | Softgels, Hard Capsules, Oil-based Formulas |
| Water-Soluble CoQ10 (CWS) | 10% / 20% / 40% | Instant cold water solubility, Clear solution | Functional Drinks, Effervescent Tablets, Gummies |
| Reduced CoQ10 (Ubiquinol) | ≥85% / 95% | Direct bioactive form, Powerful antioxidant | Premium Anti-aging, High-end Heart Health |
| Liposomal CoQ10 | Customized | Advanced Delivery System, Maximum Bioavailability | Liquid Supplements, Nutricosmetics, Oral Serums |
Deep Dive into the Three Technology Pathways
A. Standard USP-Grade Powder:
The Foundation of ReliabilityFor traditional supplement brands, our 98% Pure CoQ10 Powder remains the gold standard. Fully compliant with USP (U.S. Pharmacopeia) and EP (European Pharmacopoeia) standards, this grade offers the highest stability for lipid-based formulations like softgels, ensuring a reliable supply chain and consistent quality.
B. CWS Technology: Unlocking the Functional Beverage Market
The demand for "Drinkable Wellness" is surging. Our Cold Water Soluble (CWS) CoQ10 Powder utilizes advanced microencapsulation technology to turn hydrophobic molecules into water-dispersible particles. It ensures zero sedimentation and high clarity, making it ideal for energy drinks and functional food applications where taste and appearance are paramount.
C. Liposomal & Ubiquinol: The Frontier of Absorption
When "High Bioavailability" is your primary marketing claim, our Liposomal CoQ10 and Reduced Ubiquinol are the optimal choices.
Ubiquinol provides the body with the "already-converted" form of CoQ10 for immediate use.
Liposomal Technology acts as a protective shield, mimicking cell membranes to bypass digestive degradation and deliver the active ingredient directly to the bloodstream.

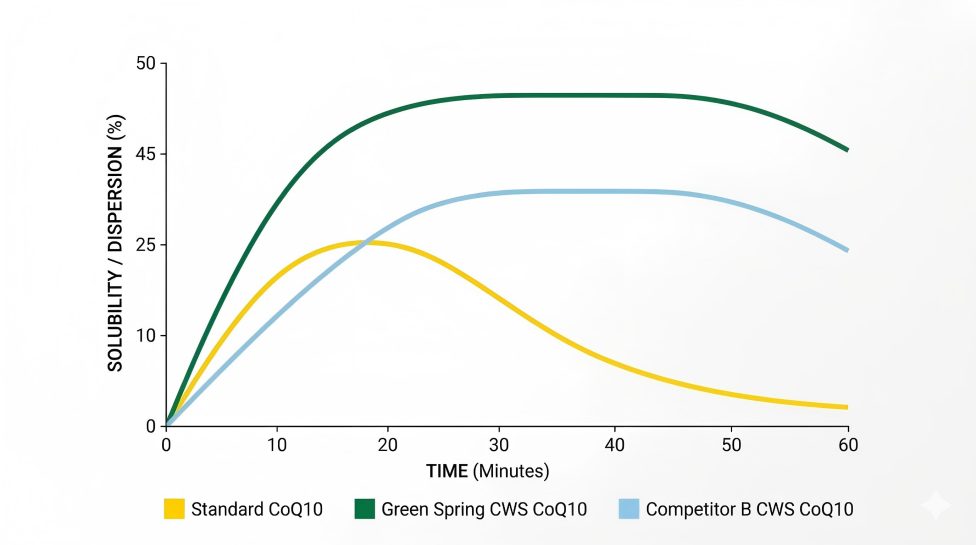
Coenzyme Q10 (CoQ10) Solubility Comparison: Standard CoQ10 vs. グリーン・春技術 Water-Soluble CWS Powder
Scientific Substance: Enhancing Product Value through Biological Mechanisms
For professional brand owners and formulators, the value of a premium ingredient lies in its ability to be substantiated by biological science. Understanding how Coenzyme Q10 functions at a cellular level allows R&D teams to design products with clear, evidence-based physiological benefits.
The Cellular Powerhouse: ATP Synthesis Support
At its core, Coenzyme Q10 is a vital co-factor in the Electron Transport Chain (ETC) within the mitochondria. For the B2B sector, this translates into a powerful selling point for Sports Nutrition and Energy Metabolism product lines:
Mechanism: CoQ10 facilitates the transfer of electrons to generate Adenosine Triphosphate (ATP).
Formulation Value: By supplying high-purity CoQ10, manufacturers can market products aimed at supporting "natural energy levels" and "cellular vitality" without relying on stimulants.
Redox Balance and Ingredient Synergy
CoQ10 is one of the few lipid-soluble antioxidants synthesized endogenously. In complex formulations, its role extends beyond its own activity:
Vitamin E Regeneration: CoQ10 has the unique ability to regenerate oxidized Vitamin E (alpha-tocopherol), creating a synergistic antioxidant network within the formula.
Stability in Nutricosmetics: In topical or oral beauty-from-within products, CoQ10 helps maintain the integrity of lipid membranes, protecting sensitive skin-health ingredients from oxidative degradation.
Bioavailability: The Science of "Effective Concentration"
The effectiveness of a finished supplement is not determined by the dosage on the label, but by the plasma concentration achieved post-ingestion. This is where the distinction between Ubiquinone and Ubiquinol becomes a critical technical choice:
Conversion Efficiency: While Ubiquinone (Oxidized form) is the most common raw material, the body must reduce it to Ubiquinol for biological use.
Target Demographics: For premium "Active Aging" formulas, providing Reduced Ubiquinol bypasses this conversion step, offering a more direct physiological pathway for consumers with compromised metabolic efficiency.
Comparative Bioavailability Chart showing plasma concentration levels of Standard CoQ10 vs. Green Spring Technology Ubiquinol and Liposomal CoQ10 over time
Quality Assurance, Compliance, and Global Supply Chain Reliability
In the botanical extract and health ingredient industry, a product is only as good as its documentation. For global B2B partners, Green Spring Technology prioritizes a "Compliance-First" approach, ensuring that our Coenzyme Q10 raw materials meet the most stringent international standards for safety, purity, and traceability.
Full Regulatory Documentation & Transparency
We understand that the regulatory approval process for your finished product depends on the quality of our data. Every batch of our CoQ10 is accompanied by a comprehensive technical dossier, including:
Certificate of Analysis (COA): Detailed testing for purity, heavy metals, and solvent residues.
Safety Data Sheets (MSDS): Ensuring safe handling and storage within your facility.
Specification Sheets: Precise technical parameters to assist your R&D and QC teams in pre-production testing.
Third-Party Testing: Periodic verification from independent labs (such as Eurofins or SGS) to ensure unbiased quality results.
International Certifications & Standards
To support your entry into global markets, our CoQ10 raw materials are produced in facilities that adhere to the highest industry benchmarks:
Pharmacopoeia Compliance: Our 98% pure powder is fully compliant with USP (U.S. Pharmacopeia) and EP (European Pharmacopoeia) standards.
Religious & Dietary Certifications: We offer Halal and 則った certified ingredients to meet the needs of diverse consumer demographics.
System Certifications: Our production follows ISO 9001 and HACCP quality management systems, guaranteeing batch-to-batch consistency and full traceability back to the raw material source.
Scalable Supply & Logistics Excellence
As a 20-year veteran in the plant extract industry, we have optimized our supply chain to mitigate market volatility and ensure long-term partnership stability:
Sustained Capacity: With a robust annual production capacity, we are capable of fulfilling bulk orders ranging from 25kg to multi-ton shipments without compromising lead times.
Strategic Stocking: We maintain strategic inventory levels to provide a buffer against global shipping delays, ensuring that your production schedule remains uninterrupted.
Global Logistics Support: Our experienced export team handles all international shipping requirements, including specialized packaging for temperature-sensitive ingredients like Ubiquinol.
-
Prev
Liposomal CoQ10 Powder: Maximizing Potency Retention and Shelf-Life Stability
-
次
Fermented CoQ10 Ushers in a New Era of Clean-Label Formulation


 英語
英語 フランス
フランス スペイン
スペイン ロシア
ロシア 韓国
韓国 日本
日本



