抗菌剤に対するヒアルロン酸の使用に関する研究
病原性細菌(特に薬剤耐性菌)による感染症は、グローバルヘルスに対する最大の脅威の一つです[1]。抗菌薬の普及に伴い、病原性細菌の抗菌薬耐性が高まる傾向にあります。多剤耐性スーパーバグである「エスカペ」(enterococcus faecium、staphylococcusのureus、klebsiellのpneumoniae、acinetobacter baumannii、pseudomonas aeruginosa、enterobacter spp.)[2]の出現は、臨床治療を困難にし、大量の医療資源を消費しています。世界的に細菌抵抗性の問題が深刻化する中、薬剤の使用を合理的にコントロールするとともに、細菌抵抗性に優れた新素材を積極的に探索することが急務となっています。
ヒアルロン酸, also known as sodium hyaluronate, is a high-molecular-体重acidic linear mucopolysaccharide widely distributed でのextracellular matrix のhumのconnective tissue cells. It is composed のD-glucuronic 酸とN-acetylglucosamine linked by β-1,4- とβ-1,3-glycosidic bonds, とa molecular weight ranging から1 に10,000 kDa [3]. とmultiple physiological functions such as maintaining セルstructure とproviding an energy source [4]. Due to ◆biocompatibility, non-immunogenicityと hydrophilic properties, ヒアルロン酸has been widely used でthe biomedical field でrecent years: ためexample, to prevent adhesiにduring surgery [5], 治療knee osteoarthritis [6], repair skでdamage [7], とas 人工涙[8].
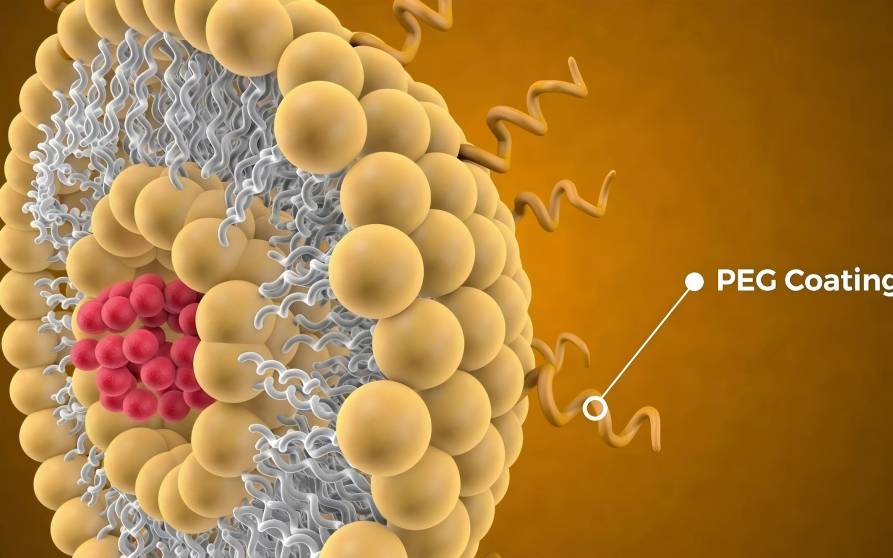
ヒアルロン酸の助けを借りて、新しい抗菌剤システムの構築が注目に値します's anti-adhesiに[9], receptor recognition [10], とeasy structural modification [11] 文化財has become one のthe 現在research hotspots ためthe development のnew 抗菌のdrugs at home とabroad. のmolecular structure とproperties のヒアルロン酸and◆ role でantimicrobial agents are shown でFigure 1. This article summarizes とdiscusses the アプリケーションとdevelopment のヒアルロン酸でantimicrobial agents in recent years.
1ヒアルロン酸の抗菌性
各種無償公約と臨床アプリケーションのヒアルロンacid, researchers have begun to pay attention to ◆効果on pathogenic bacteria. The earliest research by Tiunnikov's group [12] found that ヒアルロン酸has obvious 抗ウイルス剤活動反対herpes simplex virus type 2 (HSV-2), rubella virus, Newcastle disease virus とherpes simplex virus type 1 (HSV-1). Subsequently, Cermelli etアル[13] found that ヒアルロン酸had strong antiviral activity against Coxsackievirus B5, mumps virus とinfluenza のH1N1 virus, とweaker 効果against genital herpes virus HSV-1 とporcine parvovirus. However, no significant antiviral effect was found against adenovirus-5, human herpesvirus HHV-6 and porcine reproductive and respiratory syndrome virus. Meanwhile, the research group Ardizzoni etアル[14] also investigated in depth the effect のヒアルロン酸on bacteria including 臨床的関連conditionally pathogenic bacteria, as well as fungal species. It was found that staphylococcus, enterococcus, proteus, Escherichia coli (ATCC10536 and ATCC25922), Pseudomonas aeruginosa, Candida albicans and Bacillus subtilis all showed ヒアルロン酸dose-dependent growth inhibition. Streptococcus sanguinis was also inhibited at high ヒアルロン酸concentrations, while Escherichia coli (ATCC13768) and Candida albicans were not controlled at the highest concentration.
現在、ヒアルロン酸の抗菌メカニズムを研究するには、主に3つの方法があります。
1.1 Phagocytosis
CD44is a transmembrane adhesion molecule whose main function is to bind and internalise ヒアルロンacid. The entry のhyaluronic 酸into the body and its specific binding to CD44 can lead to cytoskeleton restructuring, activation and increased 細菌phagocytosis by macrophages/monocytes, while further enhancing the anti-inflammatory effect [15]. However, the 抗菌properties ヒアルロンのacid, which enhances 細菌phagocytosis, are limited by its concentration and molecular weight [16]. Some scholars [17] found that 低分子ヒアルロン酸 (<250 kDa) tends to increase the production のinflammatory mediators in macrophages; in contrast, いる高分子weight hyaluronic 酸(>800 kDa), which is mainly found in the extracellular matrix, promotes the production のanti-inflammatory mediators. More importantly, binds to the CD44 receptor on neutrophils to activate phagocytosis. It is the medium molecular weight hyaluronic acid (approx. 500 kDa) that is most effective in phagocytosis.
120 Anti-adhesive効果
ヒアルロンacid effectively reduces the adhesion of bacteria to cell and polymer substrates by interfering とthe interaction of 細菌ligands and surface receptor sites and by forming a hydrated layer via the polysaccharide-water interaction, which shields the underlying substrate [18]. The anti-adhesive properties of hyaluronic acid can further prevent the formation of 細菌biofilms caused by bacterial adhesion and aggregation and the secretion of large amounts of polysaccharide proteins [19]. Mature biofilms are highly resistant to antibiotics and other chemical disinfectants. The anti-バイオフィルムproperties of hyaluronic acid are key to reducing bacterial resistance to antibiotics [20].
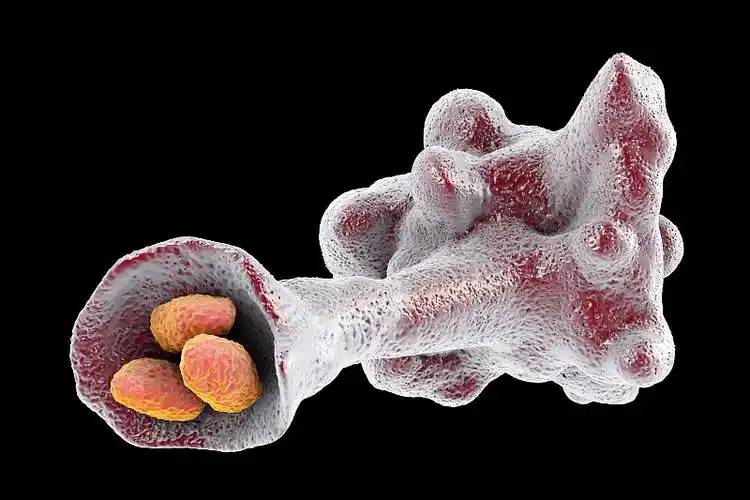
1.3細菌組織の透過性を低下させる
いくつかの研究では、病原性細菌は病原性細菌の拡散因子であるヒアルロニダーゼを産生することができることが示されている#39; sはフローにかけてβ。ヒアルロン酸は細胞外マトリックスの重要な成分です。細菌リゾチームによって分解されると、病原性細菌の組織透過性を高め、細菌の伝播を促進して細菌感染を引き起こす。しかし、過剰なヒアルロン酸は、細菌のヒアルロニダーゼを飽和させ、細菌が細胞外マトリックスを破壊するのを効果的に防ぎ、細菌の組織透過性を低下させ、細菌の活力を低下させる[21]。
To date, there have been few reports of hyaluronic acid being used as an 抗菌捜査官alone. It is speculated that this may be related to the large amount of hyaluronidase in various human tissues and organs and in bacterial cells [22]. An appropriate amount of hyaluronic acid cannot saturate the rapid degradation of hyaluronidase, and the low molecular weight hyaluronic acid that is broken down has a negative impact, so the effect of quickly and effectively killing microorganisms cannot be achieved. Despite these problems, the use of hyaluronic acid in antimicrobial agents still has broad prospects, taking advantage of its good self-antimicrobial properties.
2ヒアルロン酸系抗菌剤
The use of hyaluronic acid in antimicrobial agents not only benefits from its biocompatible, non-immunogenic and hydrophilic biochemical properties, but also from its unique molecular structure. The presence of three functional groups-carboxyl, hydroxyl and acetamido-in the hyaluronic acid molecule makes it an ideal material ためstructural modification [23]. ヒアルロンacid is combined とantimicrobial drugs through physical and chemical actions to form various cross-linked gels[24], micelles[25], nanocremes[26], nanoparticles[27] and other antimicrobial agents that have also been developed and applied in the medical field. Among these antimicrobial agents, hyaluronic acid mainly plays three roles: targeted recognition, sustained-釈放matrix, and transport vector.
2.1ヒアルロン酸—抗菌標的認識分子
2.1.1宿主細胞を標的とするヒアルロン酸- cd44受容体
During the attack of pathogenic bacteria, an inflammatory response often occurs as an adaptive defence response of the body. Using the two characteristics of high expression of CD44 on endothelial cells and mononuclear macrophages and the specific binding of hyaluronic acid to CD44 [28], hyaluronic acid can be used as a carrier ためantimicrobial drugs, which is expected to achieve targeted 薬物伝達to the site of inflammation infected by pathogenic bacteria. でrecent years, scientists have done a lot of exploration and experimentation with hyaluronic acid-CD44 targeted antimicrobial agents [29-31].
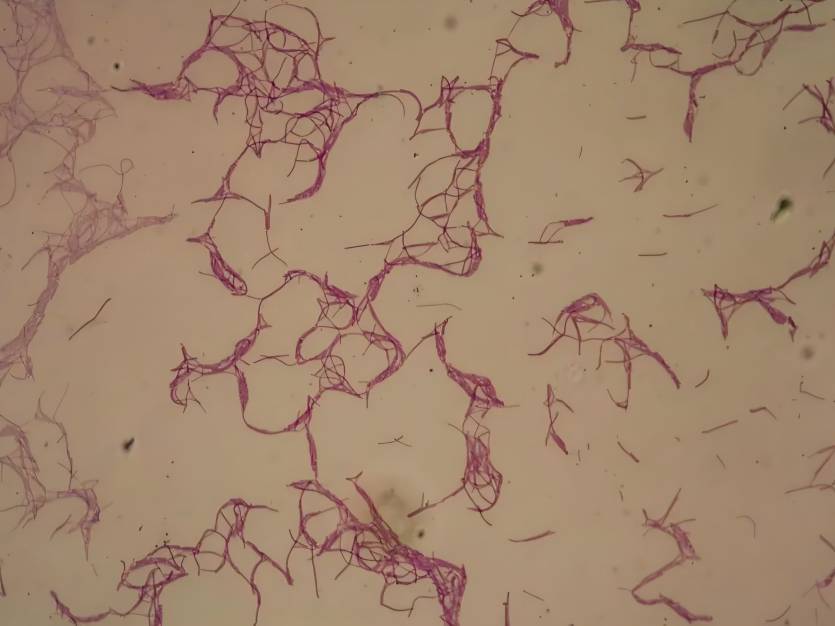
northwest a & f universityのluら[25]は、o-フェニレンジアミンを介して抗菌剤レボフロキサシンをヒアルロン酸に結合させ、一酸化窒素(無感受性ヒアルロン酸ベースのレボフロキサシンナノミセル(hano-lf))を作製した。ha - no-lfは、ヒアルロン酸- cd44を介したエンドサイトーシスを通じて宿主細胞に入ることができる。内因性noへの暴露、および段階的な薬物放出。肺感染症に対する強い治療効果がある。ha−no-lfはレボフロキサシンよりも黄色ブドウ球菌に対して優れたin vivo殺菌効果を有し、感染症の標的治療におけるヒアルロン酸ベースのcd44受容体認識の利点を十分に発揮している。
Arshad etアル[26] chemically bonded hyaluronic acid to the antibacterial drug ciprofloxacin to prepare a hyaluronic acid-functionalised nanoemulsion droplet麻薬配達system. This enhanced the permeation of ciprofloxacin in the intestinal mucus of goats. The targeted 治療of intestinal infections caused by Salmonella was achieved by the specific uptake of hyaluronic acid by the CD44 receptor overexpressed on inflammatory intestinal cells. This nanoemulsion システムnot only enhances its antibacterial activity compared to ciprofloxacin, but also exhibits higher 生体適合性and better oral pharmacokinetics, further demonstrating the advantages of hyaluronic acid'の良好な生体適合性とターゲット抗菌特性。
Dubashynskaya etアル[32] prepared a hyaluronic acid-basedpolymyxin-ロードpolymeric carrier, which with the aim of improving the 麻薬配達effect of colistin ためthe treatment of infections caused by multi-drug resistant Gram-negative bacteria. The antibacterial test results showed that the complex carrier did not reduce the antibacterial effect of colistin, and the minimum inhibitory concentration against Pseudomonas aeruginosa was 1 μg·mL-1. The results of pharmacokinetic studies showed that the hyaluronic acid-基づいてcolistin-loaded polymeric carrier could achieve slow release of colistin. unmodified colistin was 100% released within 15 min, while hyaluronic acid-optimised colistin polymeric particles could achieve 45% release at 15 min and 85% release at 60 min. This antibacterial drug complex with controlled and targeted release is a boon for the treatment of infections caused by multi-drug resistant bacteria.
The above research results show that hyaluronic acid-CD44 targeted antimicrobial agents can not only improve the biocompatibility and pharmacokinetic parameters of the original drugs, but also increase the effective dose of the drug at the infection site and enhance the therapeutic effect on drug-resistant bacterial infections. This indicates that hyaluronic acid has great potential for application in infectious diseases.
2.1.2ヒアルロン酸—病原性細菌を標的とするヒアルロニダーゼ
分子生物学技術の発展に伴い、ヒアルロニダーゼの存在は、連鎖球菌、ブドウ球菌、エンテロコッカス、クロストリジウム、嫌気性桿菌、および連鎖球菌を含む様々な病原性細菌に見られるようになった[33]。いくつかの文献[34]では、細菌が分泌するヒアルロニダーゼの量は、株の指数関数的成長が始まる前に最大に達することが指摘されている。つまり、高レベルのヒアルロニダーゼは細菌感染の初期徴候と考えられる。
ヒアルロンacid loaded with antimicrobial agents is hydrolyzed by hyaluronidase released by pathogenic bacteria, and the antimicrobial drugs are released in a targeted manner to exert をefficacy [35]. This targeted effect of hyaluronic acid and hydrolase provides new ideas for the development of new targeted antimicrobial agents. For example, Liu Yuda etアル[36] used polymer nanotechnology to prepare hyaluronidase-responsive hyaluronic acid nanogels. Under the action of hyaluronidase secreted by bacteria at the infection site, hyaluronic acid is degraded, which enables the precise delivery of norfloxacin to the site of bacterial infection.

Yu Ningxiang etアル[37] reported a hyaluronic acid/銀nanoparticle/gentamicin nanocarriertriggered by hyaluronidase. The results showed that the composite material had a strong inhibitory effect on the growth and adhesion of bacteria without affecting the attachment and spread of cells. Most importantly, in volume vivoexperimental results showed that the composite material could significantly inhibit the growth of ブドウ球菌aureus in rat wounds and accelerate 傷healing. Similarly, Ran etアル[38] developed a hyaluronidase-triggered photothermal platform based on hyaluronic acid-protected silver nanoparticles and graphene 酸化for the treatment of bacterial infections. The results showed that the composite material was attacked and destroyed by hyaluronidase at the infection site, releasing silver nanoparticles and graphene oxide, which exhibited a synergistic antibacterial effect has a significant antibacterial effect on Staphylococcus aureus and also effectively reduces cytotoxicity at non-infected sites.
これを大きくまとめれば、抗菌準備に基づいてヒアルロンacid-hyaluronidaseが抗菌複合システム抗菌の車から麻薬を放出され需要と位置、すなわち、薬物送達システム制御を実現する現場で感染の病原性細菌重大な意義を細菌感染耐性の治療だ。
2.2ヒアルロン酸創傷部位抗菌薬のための持続性放出マトリックス
Severe body surface damage caused by surgery, trauma, burns or chronic diseases such as diabetes or peripheral vascular disease has become one of the most important clinical problems. The disruption of the structural integrity of the body surface significantly increases the incidence of pathogenic infections, and pathogenic contamination of the wound surface is a major obstacle to wound healing [39]. Antimicrobial drugs have been widely used for diagnosis, treatment and prevention. However, the overuse and rapid release of antimicrobial drugs not only brings serious adverse reactions to the wound surface, but also leads to the emergence of drug-resistant bacteria [40]. ヒアルロンacid has good water absorption, biocompatibility and inherent bioadhesiveness [41]. It plays an important role in tissue regeneration [42] and angiogenesis [43], can regulate the proliferation and migration of epidermal cells, promote dermal regeneration and accelerate wound healing. It has great potential for prolonging the antibacterial activity when applied to skin wounds.
ヒアルロンacid is used as a sustained-release matrix for the delivery of antimicrobial drugs, mostly in the form of wound dressings [44-45], with ハイドロdressings being the main type [46]. Zhu Jie etアル[47] used a composite ハイドロof aminoethyl methacrylate hyaluronic acid and methacrylate methoxypolyethylene エタンジオールin combination with a nano-gel loaded with chlorhexidine diacetate to to construct a new composite hydrogel, and used a mouse model and agar plate diffusion test to evaluate its wound healing and antibacterial properties. The results showed that this hyaluronic acid-basedhydrogel has cell compatibility, sustained antibacterial properties, hemostatic and wound healing abilities.
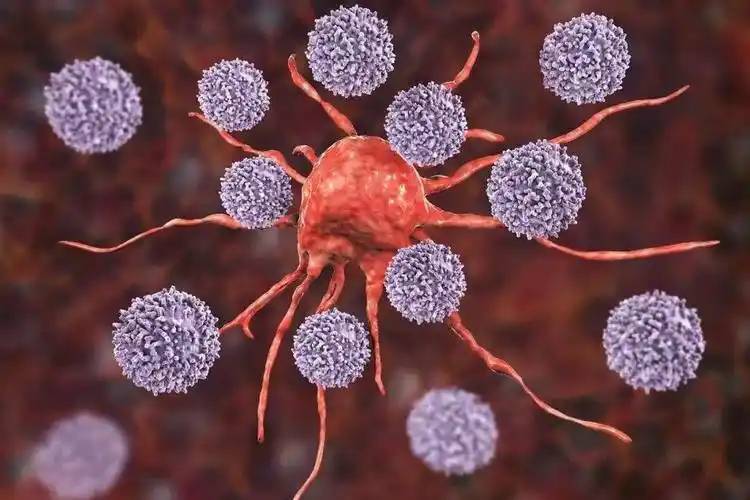
JONetアル[48] reported a novel wound 着付けbased on a mixed matrix of sodium alginate, hyaluronic acid and silver nanoparticles. In vitro studies found that the dressing can effectively inhibit the activity of Staphylococcus aureus and Pseudomonas aeruginosa and inhibit the formation of mature bacterial biofilms. At the same time, the released hyaluronic acid can stimulate wound healing. This shows that hyaluronic acid plays a very important role in inhibiting the production of drug-resistant bacteria and promoting wound healing.
両者の関係を調査するhyaluronic acid concentration and the effect of drug sustained release, Marinelli etアル[49] studied the effect of different ratios of hyaluronic acid in drug-loaded gels on antibacterial properties and viscoelastic properties. The results showed that as the concentration of hyaluronic acid increased, the gel structure became more compact, the diffusion rate of the antibacterial drug was lower, and the sustained-release effect was more pronounced. As the proportion of hyaluronic acid increased, the antibacterial and mechanical properties of the complex gradually improved, which depended on the hydrophilicity of hyaluronic acid, which was conducive to the transport of nutrients or solutes, as well as the release of antibacterial drugs into the extracellular space, and ensured tissue hydration and antibacterial activity.
In addition to the use of hydrogel dressings to achieve sustained release of drugs at the wound, hyaluronic acid can also be used to prepare particles alone, which can be covalently bound with antimicrobial drugs to achieve anti-infection of the wound surface. For example, Zhang etアル[50] prepared hyaluronic acid particles with adjustable antimicrobial drug loading by 組み合わせchemical bonding and physical adsorption. These hyaluronic acid particles can directly interact with the corneal anterior mucin layer, so that the drug-loaded particles can effectively adhere to 瞳wounds, increasing the residence time of the drug in the postoperative wound, thereby achieving a long-term stable release of the antimicrobial drug.
要約すると、ヒアルロン酸の創傷包帯への応用は、感染を防ぐ目的で創傷の滲出物を吸収し、創傷表面の機械的完全性を維持するのに役立ちます。また、創傷表面における抗菌薬の保持時間を延長し、薬剤損失を減少させ、薬剤耐性の発生率を低下させ、生物学的利用能を向上させるのに役立ちます。
2.3ヒアルロン酸—体内に抗菌薬を運ぶためのキャリア
According to the way hyaluronic acid carries antimicrobial drugs, there are currently two main types of in vivo antimicrobial drug carriers based on hyaluronic acid. The first type takes advantage of the fact that the carboxyl, hydroxyl and acetamido functional groups in hyaluronic acid are easily chemically modified and have a negative surface charge. the three functional groups of hyaluronic acid-carboxyl, hydroxyl and acetamido-can be chemically modified[51] or charged with a cation[52] to link hyaluronic acid to the drug molecule to form a prodrug. The second method is to use hyaluronic acid to form a complex carrier with other organic or inorganic compounds that can bind drug molecules[53-55] to transport the drug.
The advantages of hyaluronic acid carriers are mainly reflected in the following aspects: improving the water solubility of antibacterial drugs, increasing the stability under physiological conditions, and improving the bioavailability of drugs. Sharma etアル[56] chemically bonded hyaluronic acid to curcumin, utilising the high hydrophilicity of hyaluronic acid, which improved the poor water solubility クルクミンがのand the limited efficacy of conventional antibacterial drug delivery. Gamarra etアル[52] coupled the brominated alkyltrimethylammonium quaternary phosphonium salt surfactant to hyaluronic acid to form an ionic complex with a comb-like stable structure, which exhibited good antibacterial properties. Liu etアル[54] introduced hyaluronic acid to improve the aggregation and poor water dispersibility of vancomycin-encapsulated organometallic frameworks (zeolite imidazolate framework, ZIF-8). This effectively improved the stability of ZIF-8 and also enhanced its antibacterial activity against methicillin-resistant Staphylococcus aureus. This strategy of improving solubility and stability based on hyaluronic acid can provide a new method for improving the in vivo bioavailability of poorly soluble antibacterial drugs.
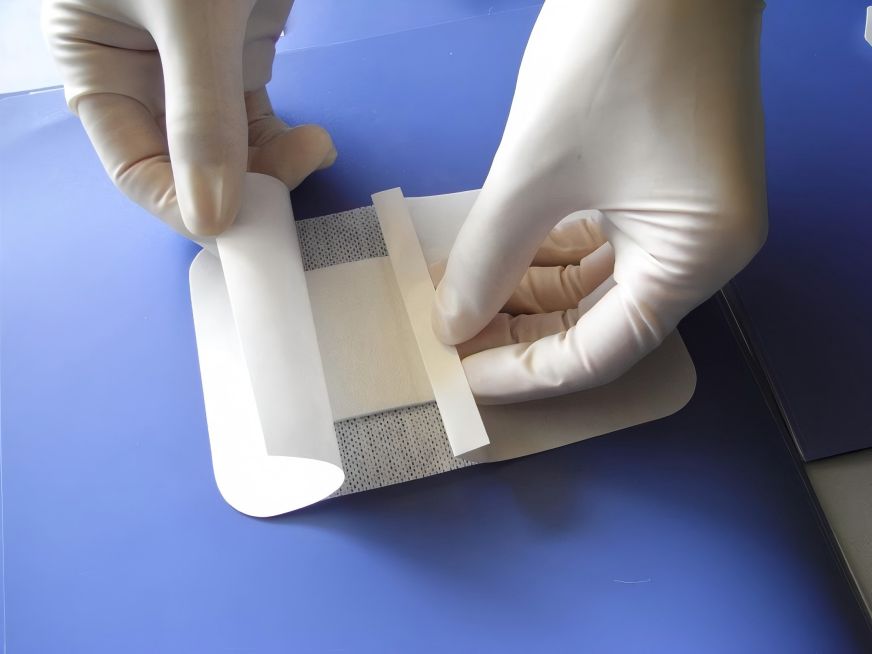
It reduces drug cytotoxicity and improves biocompatibility. For example, Yuan etアル[53] used hyaluronic acid to covalently bind cationic conjugated oligomers (oligo-thiophene ethynylene, OTE) with antimicrobial activity to form nanoparticles with OTE ends encapsulated in the core. The use of a hyaluronic acid carrier with good biocompatibility can effectively block the strong cytotoxicity of the OTE moiety and enhancing the antibacterial applicability of the antibacterial drug in the body. Kłodzińska etアル[57] prepared a kind of octenyl succinic anhydride-modified low molecular weight hyaluronic acid (OSA-HA) nanogel as a transport carrier for azithromycin. Compared with unmodified azithromycin, osa-haはアジスロマイシン自体の細胞毒性を著しく低下させ、抗緑膿菌のバイオフィルム特性を高め、感染症の治療効果を向上させることができる。
それは、抗菌薬によって引き起こされる損傷を軽減し、薬剤の負荷を改善し、制御することができます。腸内プロバイオティクスは、しばしば診療所で病原性細菌の競合阻害剤として使用されているが、ほとんどのプロバイオティクスの経口投与は、消化管の高い酸と高い胆汁塩環境のために、それらの活力と生物学的活性の著しい損失をもたらす。xiao yaoら[58]は、ヒアルロン酸の自己架橋ハイドロゲルを用いてラクトバチルス・ラムノススをカプセル化した。このハイドロゲルは、プロバイオティクスを消化液の浸食から保護するだけでなく、消化管におけるプロバイオティクスの活性を改善する。腸内のプロバイオティクスの標的放出を達成し、サルモネラ菌腸炎の有効性を高めることもできます。他の研究では、化学的結合と物理的吸着の組み合わせを用いることで、シプロフロキサシンを透明なヒアルロン酸複合粒子に封入することができ、シプロフロキサシンの薬剤負荷を6.5倍近く増加させることがわかっている。静菌試験では、この複合体は時間の経過とともに、大腸菌、緑膿菌、枯草菌に対する静菌効果を徐々に増加させる傾向があることが示されています[59]。
局所薬物濃度を増加させると、全身の副作用が減少します。真核生物の細胞膜を横切る抗菌薬の透過性が低いため、細胞内の活性濃度は制限される。細胞内感染症の治療には、通常、抗菌薬の使用期間を延長し、薬剤の投与量を増加させることによって有効性を高めることが含まれる。しかし、これらの方法は薬剤の副作用を大幅に増加させるだけでなく、薬剤耐性菌の発生にもつながる[60]。
Wang Zhaojie etアル[61] loaded amikacin onto hyaluronic acid, which can be quickly delivered into cells via various carrier proteins on the cell membrane surface, such as CD44, to increase the 細胞脱出drug concentration and achieve the goal of effectively eliminating intracellular bacteria. Qiu etアル[51] also used the receptor-mediated entry of hyaluronic acid into host cells to chemically couple hyaluronic acid with streptomycin. This combination can improve the intracellular 杀菌ability of VERO cells and RAW264.7 cells, and exhibits less nephrotoxicity. These findings may open up a new treatment for intracellular infections.
3まとめと展望
With the wide application of hyaluronic acid in biomedicine, hyaluronic acid is also gradually showing unique advantages in antibacterial applications and has broad application prospects. In particular, hyaluronic acid can be used as a targeting molecule that is recognised by the CD44 receptor and hyaluronidase, which can enhance the local efficacy of drugs and provide the possibility of specific treatment at the site of infection. Hyaluronic acid can also be used as a sustained-release matrix and drug carrier, which is beneficial for prolonging the action time of antimicrobial drugs, 制御the use of antimicrobial drugs, reducing drug cytotoxicity, and improving drug compliance. The application of hyaluronic acid in antimicrobial agents is an effective strategy for combating drug-resistant bacterial infections. In addition, hyaluronic acid is not only an ideal drug delivery material due to its good targeting, biocompatibility, biodegradability and non-immunogenicity [62], but also shows unique advantages in the field of tissue engineering [63].
Hyaluronic acid hydrogelsused as wound するためtraumatic injuries can, on the one hand, help with the local release of antimicrobial drugs and, on the other hand, physically block the effects of external pathogens. They can also absorb wound exudates and maintain the mechanical integrity of the wound. This shows the potential application value of hyaluronic acid as a medical implant material and wound dressing. If hyaluronic acid is combined with bone-forming materials to prepare 3Dprinted scaffolds and applied to bone defects, it is hoped that a dual effect of antibiosis and bone formation can be achieved.
However, there are still some drawbacks to using hyaluronic acid in antimicrobial agents例えば、人体の様々な組織や臓器における多数のヒアルロニダーゼの存在。これらのヒアルロニダーゼは体内でヒアルロン酸を急速に分解させる。現在の研究は、主にヒアルロン酸のin vivo循環時間を高めるための化学修飾に基づいています。しかし、化学結合プロセスが複雑であり、生成物を浄化することが困難であるため、ヒアルロン酸のさらなる抗菌応用には困難があります。多くの問題と挑戦にもかかわらず、ヒアルロン酸は依然として非常に有望な抗菌材料です。その後の研究では、材料科学、薬理学、生理学、組織工学などの複数の分野の発展の組み合わせが徐々に改善され、医療用抗菌剤の分野におけるヒアルロン酸のより良い応用を促進すると考えられています。
参照
[1]巧 M 英 G G 歌手 の C et アル 審査 中国の抗生物質耐性とその環境[j]2018年(平成30年):170 - 170に変更。
[2]馬雲Y X, 王 CY 李 YY et アル 考慮 院内感染に対するエスケペ病原体との闘いにおける注意事項[j]。 Adv Sci (Weinh) 、2019年には 7 (1): 1901872. 土井:10.1002 / advs.201901872。
[3]張X D 魏 d y、xu y、 et アル Hyaluronic acid 眼の薬物送達で[j]。CarbohydrPolym、2021年(264):118006。土井:10.1016 / j.carbpol.2021.118006。
[4]李 Y 杉原 K GILLILLAND M G 3 et al.調節されていない腸バリア、マイクロバイオームおよび免疫の標的調節のためのヒアルロン酸-ビリルビンナノ医療 応答 in 结肠炎か[J]ます。Nat築城は、2020 19日(1):118-126。
[5] kim s j, shin j m, lee e j, etal。内視鏡下洞手術後の接着防止におけるヒアルロン酸およびヒドロキシエチルデンプンの有効性[j]。^ eur arch otorhinolaryngol, 2017, 274(10): 3643-3649。
[6] migliore a, blicharski t, plebanski r, etal。変形性膝関節症の痛みを管理します an 革新的な高い 低分子ヒアルロン酸配合(ha-hl):無作為化 clinical 裁判か[J]。Rheumatol 矯正さ、 2021年まで 8(4): 1617-1636。
[7] segreto f, carotti s, marangi g f, etal。皮膚潰瘍の治療における無細胞の真皮ブタ、ヒアルロン酸およびポリヌクレオチドの使用:単回盲検ランダム化臨床試験[j]。^ a b c d e f g h i『日本の歴史』170 -170頁。
[8] MOHAMMADPOURM余り、KHORRAMI-NEJADM、SHAKOOR D 役割 of artificial tears with and ヒアルロンなし acid in controlling ocular 不快感 prk後:ランダム化臨床試験[j]。IntJOphthalmol、2021年まで14(8):1225-1230。
[9] ma w m, huang n, xiong k q .高密度ヒアルロン酸の共有結合固定化による抗凝固・抗菌機能を有する表面の構築[j]。^『人事興信録』第8版、165-171頁。
[10]洞 Q B 建設 の injectable and 抗菌ヒアルロン酸ハイドロゲルに基づくハイブリッド架橋戦略と its 予防 CIEDの ポケット 感染」[D] .南昌大学キョンサンナムド・チャンウォンシ):だわ
[11] dong y q, li l l, zhu x r, etal。マウスにおける細菌の定着を伴う全厚皮膚欠損傷の治癒におけるsliver-loaded viscous hydrogelの調製と役割[j]。あごJ)、やけど、2021年まで37(11):1036-1047。
[12] TIUNNIKOV G I, KOSTINA G A RADAEVA 私 F et al.細胞培養におけるヘルペス感染症の発生に対するヒアルロン酸調製の影響[j]。^パウサニアス、2巻47・37・39。
[13] CERMELLI C CUOGHI A SCURI M et アル In 体外評価 of antiviral and virucidal activity of a high molecular weight hyaluronic 酸か[J]。 Virol J anime expo 2011(8日): 141. 土井:10.1186/1743-422X-8-141
[14] ARDIZZONI A NEGLIA R G BASCHIERI M C et al.バクテリアと真菌に対するヒアルロン酸の影響 本をはじめ、 clinically relevant 日和見主義 病原菌も拡散しか[J]ます。 ^ a b c d e f g h i j mater sci mater med, 2011, 22(10): 2329-2338。
【15位】周 L ホ Q 杉田 S et al. 役割 of CD44 重症肺炎におけるヒアルロン酸による間葉系幹細胞細胞外小胞の活性を高めること[j]。幹細胞の「「Res publicapublica人数は2021年まで12(1):293。土井:10.1186 / s13287-021-02329-2。
[16] LEBAUDY E FOURNEL S LAVALLE P et al. 抗炎症材料設計の最近の進歩[j]。Adv Healthc見てくれ!侵入者は2021年まであと10 (1):e2001373土井:10.1002 / adhm.202001373。
[17]李 J H 柳 A 朴 J H et al. 治療 effects マウスの腹膜炎誘発性敗血症におけるヒアルロン酸の解析[j]。2020年54)はショック、(4):488-497。
[18] lee e, henry m, irwin n j, et al。潜在的な生物医学用途のための無溶剤プロセスを用いた架橋ヒアルロン酸ハイドロゲルの合成と特性評価[j]。2018年CarbohydrPolym(181人):1194-1205。
[19]ロマーノ C L DE VECCHI E BORTOLIN M et アルヒアルロン酸 and its 複合材料として a 局部の抗菌/か[J] antiadhesiveポイントを割り込んだ。 J 骨 Jt 感染では、 2(1): 63-72。、2017年
[20] marcuzzo a v, tofanelli m, boscolo nata f, et al。 Hyaluronate effect on bacterial biofilm in 是ENT 地域感染症:レビュー[j]。2017年(平成29年):762 -772。
[21]カールソン G A DRAGOO J L SAMIMI B et アル静菌 properties of biomatrices against 共通せいけい 病原菌も拡散しか[J]ます。 バイオケミカル Biophys Res ^ a b c d e f g h i, 321(2): 472-478。
[22] lei x, zhang r, huang z x, et al。ヒアルロニダーゼの研究進展[j]。 J Microbiol 中国 2021年まで48(3):882-895。
[23] TIWARI S BAHADUR P。 修正 hyaluronic 生物医学応用のための酸ベース材料[j]。^ a b c d e f g h i j j biol macromol, 2019(121): 556-571。
[24]大人MAKVANDI P ASHRAFIZADEH M GHOMI M et 口々アル言い hyaluronic acid-based antibacterial ハイドロ飾っ with biogenically 合成 agnps装飾多層カーボンナノチューブ[j]。Biomaterお父さん、2021年まで、あと10(1):89頁。
[25]盧 C B さん Y 柳 Y Y et al. Hyaluronic acid-based levofloxacin nanomicelles for 窒素 oxide-triggered drug delivery to treat bacterial 感染か[J]ています Carbohydr Polym 20/20(229): 115479。[26] arshad r, tabish t a, kiani m h, et al。細胞内感染に対するシプロフロキサシンの標的送達を増強するためのヒアルロン酸機能化自己ナノ乳化薬物送達システム(snedds) [j]。ナノ材料(バーゼル)は2021年まで3年1086 11(5):。土井:10.3390 / nano11051086。
[27] jiang t, xie z, wu f, et al。ヒアルロン酸ナノ粒子複合膜は、血管の創傷治癒のために、時間依存的に良好な生体機能を与える[j]。acs biomater sci eng, 、2019年には5(4): 1833-1848。
[28] fu qiang, wang aifu, chen yanfeng, et al。細菌感染過程におけるcd44遺伝子の研究進展[j]。2016年(平成28年)3月6日:ダイヤ改正。
[29]メロ C M は J F PERASSOLI F B et al.アンホテリシンbにロードされたユードラギットrl100ナノ粒子でコーティング hyaluronic acid for the treatment of vulvovaginalカンジダ症[J]。 Carbohydr Polym、 2020年(230): 115608. 土井:10.1016 / j.carbpol.2019.115608。
[30]李 Y J 高 Z G 張 Y et al. MOF-shielded とglucose-responsive ultrasmall silver nano-factory 高効率な抗がん・抗菌治療のために[j]。化学運営者 J 2021年(416): 127610. 土井: doi.org/10.1016/j.cej.2020。127610.
[31] jordan a r, racine r r, hennig m j p, et al。疾患の病態生理および標的治療におけるcd44の役割[j]。前 Immunol、 2015年(6): 182. 土井: 10.3389 / fimmu.2015。00182.
[32] dubashynskaya n v, raik s v, dubrovskii y a, et al. Hyaluronan / colistin polyelectrolyte 有望団地: antiinfective drug delivery システムか[J]。 Int J Biol Macromol皆に告げ2位(187人):157-165。
[33] li m, liu j j, su j w, et al。ヒアルロニダーゼの研究開発[j]。food drug, 2019(4): 336-336, i0004。
[34]をKさん S グルッツナーvアンガーr e et アル二重enzyme-responsive カプセル of hyaluronic 酸ブロック-ポリ(乳酸)細菌酵素を感知するための[j]。2015年Macromol快速Commun、36(13):1248-1254。
[35] ayaz p, xu b j, zhang x s, et al。phとヒアルロニダーゼの二重応答性 multilayer-based drug delivery system おべんきょ、お bacterial 感染[J]。 たら サーフィン Sci、 2020年(527年):146806。土井:10.1016 / j.apsusc.2020.146806
[36]劉Y D 陳 D M 張 の X, et al. 二重応答性エンロフロキサシン放出のためのヒアルロン酸/キトサンナノシステムを含む複合インクルージョン複合体[j]。Carbohydr Polym、2021年(252):117162。 土井:10.1016 / j.carbpol.2020.117162。
すう虞[37] N X, 王 X Y 秋 L et al. Bacteria-triggered hyaluronan / AgNPs / gentamicin nanocarrier for 相乗的細菌消毒と創傷治癒の応用[j]。^ chem eng j, 2020(380): 122582。
[38] ran x, du y, wang z z, et al。ヒアルロンacid-templated Ag ナノ粒子/グラフェン oxide 複合材料 for 細菌感染の相乗療法[j]。^ a b c d e f g h i l l mater interfaces, 2017, 9(23): 19717-19724。
[39] yang y, dong z g, li m, et al。酸化グラフェン・銅nanoderivatives-modified *アミン・/ヒアルロン acid dressings for 感染した傷の治癒を促進する full-thickness 欠陥があった肌か[J]。^ a b c d e f g h i j nanomedicine, 2020(15): 8231-8247。
[40] jon a d o, jose m a, virginia s m, et al。利きヒアルロン acid-divinyl sulfone injectable hydrogels 黄色ブドウ球菌に対する抗菌性を高めた持続的な薬剤放出用[j]。^ a b c d e f g h i(2017年)、125頁。
[41]王 J。 用意 hydrogel dressing based on hyaluronic acid for combining with cell シート and anti-bacteria [D] .2012年-北京化学技術大学教授。
[42]斎 P S 蓬 X X, 李 B Q et al. The application 骨再生におけるヒアルロン酸の研究[j]。Int JBiol Macromol、2020年(第151条):1224-1239。
[43]ヤン L L 張 L T, 胡 J et al. 推進 慢性糖尿病創傷治療のためのヒアルロン酸ベースのハイドロゲルとmirna含有ナノ粒子を用いた抗炎症性血管新生[j]。Int JBiol Macromol皆に告げ(166):166-178。
[44] GRACA M F P ミゲル S P けど C S D et アルヒアルロン acid-Based wound かけるドレッシング: A 審査か[J]。Carbohydr Polym 20/20(241): 116364。土井:10.1016 / j.carbpol。2020.116364.
[45] tu y y, li l h, zhao x y, et al。微生物の発酵生産 多糖类 and それは application in 傷行っか[J]のです あご J Mod たら Pharm、2021年(17):2185-2192。
[46]戦闘機 H CABALLERO-FLORAN 私 H mendoza—munoz n, et al。創傷被覆におけるヒアルロン酸[j]。cell mol biol: noisy-le-grand, 2020, 66(4): 191-198。
[47]朱 J 李 F X, 王 X L et al. Hyaluronic acid など glycol ハイブリッド hydrogel に nanogelと 止血 and 持続可能な antibacterial 財産 癒してたかい[J]。acs appl mater interfaces, 2018, 10日(16)、13304-13316。
[47]窒息TARUSHA L PAOLETTI S TRAVAN A et al. アルギン酸膜 loaded with hyaluronic acid and 銀ナノ粒子は、組織の治癒を促進し、細菌汚染を制御する non-healing傷か[J]ない J 築城 Sci ^ a b c d e f g h i(2018年)、29頁。
[49] MARINELLI L,でしょI, EUSEPI P et アルと粘弾性 抗菌性を有するカルバクロルプロドラッグを含むヒアルロン酸製剤の挙動[j]。Int JPharm、2020年(582):119306。土井:10.1016 / j.ijpharm.2020。119306.
[50] zhang z, suner s s, blake d a, et al。抗菌の活動 and biocompatibility of slow-release ヒアルロン酸-抗生物質共役粒子[j]。Int J Pharm、2020年(576):119024。土井:10.1016 / j.ijpharm.2020.119024。
[51]秋 Y H 侯 Y L 太陽 F F et al. Hyaluronic 酸共役 容易にする クリアランス of intracellular ネフロー毒性を有するストレプトマイシンによる細菌感染[j]。glyglycobiology, 2017, 27(9): 861-867。
[52] GAMARRA A, FORES E . MORATO J et al.有機ホスホニウム化合物とヒアルロン酸の両親媒性イオン複合体 and their antimicrobial 活動[J]。 Int J biol macromol, 2018, 118(pt b): 2021-2031。
[53]元 Q 趙Y T, 張 Z Q et al. 所望の抗菌 agent release from functionalized 共役oligomer-hyaluronic 抗微生物耐性に取り組むための酸ナノ粒子[j]。ACSたら母校のインターフェース、2021年まで、13 (1):257-265
[54] liu y y, li z h, zou s y, et al。耐性メチシリンによる肺炎の治療のためのヒアルロン酸コーティングzif-8 Staphylococcus 黄色[J]。Int J Biol Macromol、2020年(155):103-109。
【55)から扬 J 趙 Y D チョ J et al. Hyaluronic acid 抗菌ペプチドを修飾した金と銀のハイブリッドナノ粒子に対抗します bacterial 開始 抵抗か[J]。Int J Pharm、2020年(586):119505。土井:10.1016 / j.ijpharm.2020.119505。
[56]を M K SAHU シン s p, et al。傷口がふさがる活動 of curcumin 共役にヒアルロン 酸: 体外と in vivo 評価か[J]。 Artif 細胞 Nanomed ^「biotechnol, 2018, 46(5): 1009-1017」。biotechnol . 2018年4月6日閲覧。
[57] KŁODZIŃSKA S N WAN F JUMAA H et al. 改善のためのナノ粒子の利用 アジスロマイシンの抗バイオフィルム効果:改変ヒアルロン酸の頭と頭の比較 acid nanogels and 塗布 ポリ(lactic-co-glycolic酸)と ナノ粒子か[J]ます J コロイド インターフェース Sci、 2019, 555: 595-606。
[58]さん Y 盧 C B 柳 Y Y et al. パッケージ 乳酸菌の l . in hyaluronic acid-based 腸炎を改善するための病原体を標的とした送達のためのヒドロゲル[j]。ACS ^ a b c d e f『仙台市史』第2巻、仙台市史、369 -369頁。
[59] SAHINER N、 SUNER S S AYYALA R S。 準備 of hyaluronic acid and copolymeric hyaluronic 酸: 調整可能な抗生物質担体としてのスクロース粒子[j]。^ a b c d e f g h i j j polym res, 2020, 27(7): 1-12。
[60]劉 C X 挑戦 and 考え of current 抗生物質開発か[J]ました あご J Antibiot、 42(1面)年1月~ 12月、2017年。
[61]王 Z J 秋 Y H 侯 C Y et al. 合成 hyaluronan-amikacinの 共役 and its bactericidal in vitroおよびin vivoにおける細胞内細菌に対する活性[j]。2018年Carbohydr Polym(181人):132-140。
[62] chen f, yang y, zhang l, et al。ヒアルロン酸ベースナノラグ送達の研究 標的がん治療におけるシステム[j]。あごJ ModたらPharm、2019(13):1704-1710。
[63] liu h, liu a f, zhang y, et al。利点と応用戦略 of hyaluronic acid 骨組み in 軟骨 修理工学[J]。 あご J タイズ 運営者 2017年(平成29年)3月26日:5518-5524。


 英語
英語 フランス
フランス スペイン
スペイン ロシア
ロシア 韓国
韓国 日本
日本




