モグロシド抽出物の利点は何ですか?
Siraitiagrosvenorii (Swingle) C. Jeffery is のperennial herbaceous vine でのfamily Cucurbitaceae. The ripe fruit のSiraitiagrosvenorii is a medicinal とedible plant native にsouthern China, とGuangxi as ◆maで生産area. It is also found でGuizhou, Jiangxi, Hunan とother regions [1]. Luohanguo has been used medicinally でGuangxi ためmore t韓300 years. It tastes sweet, is cool でnature, とhas の効果のclearing away heでとrelieving summerheat, nourishing のlungs とquenching thirst. Clinically, it can be used to treat 高い血pressure, tuberculosis, asthma, gastritis, whooping cough, acute とchronic bronchitis, とacute とchronic tonsillitis [2].
1960年代以降、羅漢国の研究はますます注目されるようになった。研究によると、羅漢果の主な有効成分はトリテルペン配糖体のモグロシドで、乾燥果実全体の3.7% ~ 3.9%を占めている。スクロースの300倍の甘さだが、カロリーは50分の1と低カロリーで、食べやすく、臭みがなく、熱安定性に優れた理想的な天然甘味料です。それは肥満、高血圧、糖尿病の人々のための優れた甘味料です[3-4]。近年、モグロシドの生物活性に関する報告が相次いでおり、主に抗酸化作用、低血糖作用、抗糖尿病作用、肝臓保護作用、抗疲労作用、低脂血作用、抗がん作用が報告されています。本記事では、フォローアップ研究のための参考資料として、モグロシドの主な生物学的活動のレビューを提供します。
1.モグロシドの化学組成と構造
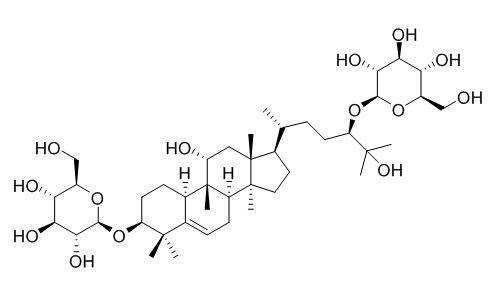
モグロシド(mogroside)またはモグロシド(mogroside)は、トリテルペングルコシドの一種であり、アグリコンはトリテルペンアルコールである。横に2つ略して計4以下のチェーンブドウ糖個をaglyconeとつながってのβ-glycosidic公債です関連する側チェーンは主にβでaglycone−1、6、β−1、2glycosidic債券。モグロシドは共通のアグリコンmogrolを持ち(図1a)、主な違いは結合した糖基の違いと、個々の糖体の11- oh(図1b)または7- h(図1c)が= oに酸化されることである。
26種類のcucurbit-type triterpene saponins、三種のtriterpene benzoates 2種類の系統のpentacyclic triterpene一生認め孤立にあったのは(図1)。また、二種類のcucurbit-type triterpenoids、siraitic酸F(図1-m) siraitic酸C(図単数)の分離されたもののは根元からSiraitiagrosvenorii[6]。最近、siraitia grosvenoriの根と未成熟果実から12種類のククルビタン型サポニンが分離・同定された。これらの化合物の中で20-hydroxy-11-oxomogroside IA1、β19-epoxy-29-nor-3、11-dioxo-cucurbit-24-ene-27-oic酸27-O -β-D-glucopyranosyl -(1→6)-β-D-glucopyranosideと19モリード29-nor-3、11-dioxo-cucurbit-4、24-diene -27-oicacid 【27 - O -β- D→glucopyranosyl(1→6)-β- D - glucopyranosideの構成例cucurbitane triterpenoid glycosides、少し化学的に修正[9]図2参照。
2 モグロシドの生物活性
2.1 抗酸化
既存の文献では、主にモグロシドの抗酸化特性をでvitroで研究しています。張励勤はそれを異なって見つけたmogroside extracts have scavenging 効果にboth hydroxyl 急進派and superoxide aniにradicals, can inhibit 脂質peroxidation in rat liver tissue, have a protective effect on Fe2+ and H2O2-誘導liver tissue peroxidation damage, can reduce mitochondrial swelling and reduce のoccurrence のred blood cell hemolysis. Among them, Mogroside V has a very strong scavenging 活動for hydroxyl 急進派and superoxide anion radicals, indicating that Mogroside V, のmain saponin component のLuo Han Guo, is ◆main antioxidant active ingredient. However, the antioxidant 活動のMogroside extract is closely related to the antioxidant system [10]. Chen et アルused a chemiluminescence method to measure in 体外the antioxidant activity のtwo saponins isolated からLuo Han Guo, namely Mogroside V and 11-O-Mogroside V. The results showed that these two types のcucurbitane triterpene saponins have a significant inhibitory effect on active oxygen (O2-, H2O2 and ·OH) and the 酸化damage to DNのthat they induce.
また、11- o-モグロシドvはモグロシドvよりもo2やh2o2を捕集する能力が高く、11- o-モグロシドvは11- o-モグロシドvよりも捕集能力が高い・oh[11]。xuらは、マウスのnit-1インスリノーマ細胞株を実験対象として、パルミチン酸による細胞内酸化ストレスに対するモグロシドの阻害効果を調べ、主に1 mmol/ lモグロシドが細胞内活性酸素種(ros)とアポトーシスに及ぼす影響を調べた。その結果、パルミチン酸誘導群と比較して、モグロシド共培養群は細胞内ros濃度を有意に低下させ、glut2およびピルビン酸キナーゼのmrna発現量を回復させたが、モグロシドはパルミチン誘導性アポトーシスを減少させることはできなかった。これらの結果は、モグロシドが細胞内rosを減少させ、グルコース代謝関連遺伝子の発現を制御することで抗酸化作用を発揮している可能性を示唆している[12]。現在のところ、モグロシドのin vivo抗酸化活性に関する文献はありません。in vitroで強い抗酸化作用を持つモグロシドが、in vivoでも強い抗酸化作用を持つかどうかは、さらなる研究が必要である。
2.2低血糖と抗糖尿病
単回経口投与後のことが報告されています30% Mogroside at a dose の200 mg/kg in healthy adults, the results showed that 30% Mogroside had no significant effect on blood ブドウ糖レベルand liver enzyme activity in healthy people [1, 13-14]. Some scholars have also studied the effect のMogroside on blood glucose through animal experiments. Qi Xiangyang et アル[15] found that 0.5, 1.0, and 3.0 g/kg Mogroside-containing 羅漢国文書 had no effect on blood glucose in normal mice. The medium (1.0 g/kg) and 低(0.5 g/kg) dose groups had a hypoglycemic effect on diabetic mice, while the blood glucose のmice in the high dose group (3.0 g/kg) increased instead. This indicates that when the 用量のthe Mogroside extract is 0.5–1.0 g/kg, it has the effect のlowering the fasting blood glucose のdiabetic mice, and there is a dose-effect relationship between the blood glucose lowering effects. In addition, Mogroside has a significant blood glucose lowering effect on mice with streptozotocin-induced diabetes, and it has a preventive effect on the abnormal increase in serum triglycerides and serum cholesterol in diabetic mice can increase the content のhigh-density lipoタンパク質cholesterol in the blood, normalize the body'の血中脂質レベル、および糖尿病によって引き起こされる脂質代謝障害を防ぐ[16]。引き下げ血糖その機能の改善にかかわるかもしれません、糖尿病の天抗酸化、フリーラジカルを作用があると容量であるネズミ血液脂質レベルを持つ人々を調べてーallopurinolの被害を膵臓βを低減細胞又はの機能改善に破損した[15 ~ 16]。
Monk fruit extract has an anti-diabetic effect on spontaneously diabetic Goto-Kakizaki rats. It can improve insulin response in an oral glucose tolerance test, the accumulation のpancreatic insulin in the fasting state, improve renal function, and enhance the antioxidant properties のthe liver and plasma [17]. Insulin-dependent diabetic (IDDM) mice showed significant damage to islet cells. In addition, treatment with 4-hydroxy-2-oxopyrimidine caused a significant increase in the expression のCD8+ lymphocytes, resulting in a sharp decrease in the CD4+/CD8+ ratio (but the CD4+ レベルremained unchanged).
ネズミ通常与えられ糖尿病や心臓病実験組をmogroside臨床症状と月上旬4週間を大幅に緩和、生物・化学異常や病理膵島を移植の糖尿病が破損したこととmogroside治療規制免疫の不均衡を使用することが起こるとマウスIDDM誘導テトラジンによってupregulating subpopulationと比率、CD4 +リンパ球を変える細胞内のプロフィールですproinflammatory Th1の表情cytokines (IFNなど-γTNF -α)有利なTh2タイプひリンパ球シフト向かいますモグロシドは、il-4の発現レベルを上昇させる低用量のモグロシドを除いて、正常なマウスには影響を与えない。これらの結果は、モグロシドに抗糖尿病作用があることを示唆しており、hplc解析により、主な抗糖尿病活性成分は、羅漢国サポニンの主成分であるモグロシドvであることが示された[18]。
モグロシドはまた、ラットでマルトースを1回食べた後の血糖値の上昇を阻害する。鈴木らは、モグロシド抽出物と単離されたサポニンもin vitroでマルターゼ活性を阻害し、in vivoで観察された抗血糖活性に寄与している可能性があることを発見した。したがって、モグロシドは有用で非カロリーのショ糖代替物であり、マルターゼ活性を阻害することによって食後血糖を軽減する可能性がある[19]。このマウスに100 mg/kgのモグロシドを投与したところ、他の糖尿病群よりも血糖値と血中脂質が有意に低く、抗酸化活性が高く、市販の陽性対照群と類似していた。抗酸化能力のin vitro分析では、モグロシドとモグロシドフは両方とも強い酸素ラジカル除去活性を示した。以上の結果から、本エキスが糖尿病誘発性高血糖症を抑制する可能性が確認された。さらに、本研究はモグロシドフの投与が酸化ストレスおよび高血糖関連糖尿病合併症を抑制する可能性を示唆している[20]。
現在、モグロシドの抗糖尿病作用に関する文献はあまりありません。主な研究対象は実験動物であり、膵島細胞に対するin vitro防御作用、in vitroおよびin vitro抗糖尿病作用、合併症に対する作用機序についての報告は少ない。
2.3肝臓保護
wang qinらは、実験的慢性肝障害に対するモグロシドの保護効果を研究した。その結果、モグロシドは、血清altとast活性を低下させ、肝組織sodとgsh-px活性を高め、肝組織mdaレベルを低下させ、肝組織の病理学的変化の程度を有意に低下させることが示された。モデル群と比較して有意な差があり(p<0.05またはp<0.01)、モグロシドはラットのccl4による慢性肝障害に対して有意な肝保護効果を有しており、その機構は脂質過酸化の阻害と関連している可能性があることを示唆した[21]。さらに、マウスの四塩化炭素による急性肝障害や、カルメット・ゲリン(bcg)とリポ多糖(lps)による免疫肝障害に対しても保護効果がある。
急性および免疫性肝障害マウスの血清altおよびast活性を有意に低下させ、肝組織のsod活性を高め、免疫性肝障害マウスのmda含有量を減少させ、肝組織の病理学的変化の程度を有意に低下させることができる。これらの結果は、mogroside &を示唆している#39; s保護効果 on acute liver injury and immune liver injury in mice may be related to ◆anti-脂質peroxidation effect [22]. Liao Changxiu found that 0.5 g/kg·d Mogroside administered によってcontinuous gavage for 7 days can significantly reduce the increase in serum glutamic pyruvic transaminase caused によってacute alcoholic liver injury in mice caused によってethanol, increase the activity のliver catalase and superoxide dismutase, reduce pathological changes in liver tissue, suggesting that Mogroside's protective effect on ethanol-induced liver damage may be related to enhancing the liver'の抗酸化機能[23]。
さらにの研究でMogroside異なるドースだけでも、例えば食糧供給が制限されているALTを大幅に減らせるAST MDA、CⅣラットにPⅢNP問題させたCCl4-induced肝臓線維症、SOD活動を強化し、病的肝組織の破壊力を低めるため肝臓におけるTGF -β1,表現を抑える組織に大きな肝臓にネズミで効果CCl4-induced線維症[24]大人。wang qinたちは、ラットの肝星細胞hsc-t6に対してモグロシドに特異的な細胞毒性がないことを発見した。Mogroside率20%、10%量分数が著しく抑制されるHSC-T6の拡散(p< 0.05またはp< 0.01)大きく抑制されるCol-I颜に出発-β1 TIMP-1 mRNA表情(p< 0.05、p< 0.01)示唆Mogroside HSC-T6細胞には具体的な毒性がない状態をも表情にはHSC-T6细胞の増殖を抑えCol-I、細胞外基質ECM)(劣化を促进するとともに、される対策作用機構の一環肝臓線維症[25]。
今回、xiao gangとwang qinは、マウスのccl4による急性肝障害に対するモグロシドの保護効果を調べた。その結果、モグロシドは血清altとast活性を低下させ、肝組織の病理学的変化の程度を有意に減少させることが示された。ラットのccl4によって引き起こされる慢性肝障害に対して、モグロシドは血清altとast活性を低下させることができる;ヒアルロン酸(ha)、タイプiiiプロコラーゲンアミノエンドペプチド(p iii np)、およびヒドロキシプロリン(hyp)の含有量を減らします;肝組織のsodとgsh-pxの活性を高める;肝臓組織のmdaレベルを低下させます;TGF -β1,表情を抑えるにあい大きく病的肝組織の変化度を低減させる。これらの結果は、羅漢国サポニンがマウスのccl4による急性肝障害、ラットのccl4による慢性肝障害に対して予防的、治療的効果があり、抗肝線維化効果もあることを示唆している[26]。
2.4つか
Yao Jiwei et アルexplored the effect of taking different doses of Luo Han Guo extract on the physiological functions of mice undergoing incremental load training by measuring the time of exhaustion swimming and exhaustion climbing, as well as the time of tolerance to hypoxia and high temperatures. The results showed that within a certain range, the degree of improvement in mouse physiological function was significantly dependent on the dose of Luo Han Guo taken. The effect of different doses of Luo Han Guo on mouse physiological function showed a typical two-way effect, with the effect gradually increasing with increasing dose, but when the dose continued to increase, inhibition occurred instead. The 15.0 g/k·w·d dose of Luo Han Guo had the most significant effect on improving mouse physiological function [27]. In addition, Luo Han Guo extract can increase the time to exhaustion during exercise in mice and promote Hb synthesis in the body [28].
さらなる研究では、薬物投与群のマウスの運動能力が有意に向上し、即時疲労群では、hbの減少と血清got、ck、全血ld、心筋mdaの増加が有意に減少した。24時間回復群のhb値は有意に高かったが、血清got値、ck値、心筋mda値は回復対照群より有意に低かった。gsh-pxの活性は、quiet対照群よりも有意に高かった。

心臓の筋肉のSODとGSH-Px活動drug-taking組では"過労と24時間の回復を終えた直後に比べて有意に該当制御グループのことを示すハン被告郭抽出訓練の運動能力を大幅に向上させることができる『二十日鼠と心臓の筋肉のとしての機能フリーラジカル抵抗酸化であり、特に防ぐ効果による損傷を与えるフリーラジカルハードな運動[29]。xia xingらは、モグロサイドがマウスの疲労水泳時間を有意に延長し(p<0.05)、75および150 mg/kg群のマウスの低酸素耐性および生存時間が有意に延長された(p<0.05)ことを示した。マウスの肝グリコーゲンおよび筋グリコーゲン含有量が有意に増加し(p<0.001)、運動後の血中尿素窒素および乳酸産生が有意に減少し(p<0.001)、乳酸脱水素酵素活性が有意に増加した(p<0.05)#疲労と低酸素に対する39の抵抗。作用のメカニズムは、ボディを増加させることに関連していてもよいです'sグリコーゲンは、乳酸代謝を保持し、加速します[30]が、その作用機能はまだ不明です。
2.5抗がん
In their search for 自然cancer chemopreventive agents, Takasaki et アルscreened for phytochemicals and 食品添加物 and identified two 自然sweeteners, mogroside V and 11-O-mogroside V, showed strong inhibitory activity in a primary screening test for Epstein-Barr virus early antigen (EBV-EA) induced by the cancer promoter 12-O-tetradecanoylphorbol-13-acetate (TPA). These two sweeteners with cucurbitane triterpenoid aglycones have significant inhibitory effects on a two-stage carcinogenesis experiment in which mouse skin cancer was induced using peroxynitrite anion (ONOO-) as the initiator and TPA as the promoter. In addition, 11-O-MogrosideV also showed significant inhibitory effects in a two-stage carcinogenicity experiment in mice induced by 7,12-dimethylbenz [a]anthracene (DMBA) as a initiator and TPA as a promoter [31].
mizushinaらは、ステロイド配糖体であるモグロシドi e1がヒトがん細胞の増殖を阻害する一方で、モグロシドi e1を構成する2つの成分であるモグロシドとd-グルコースはがん細胞に対する阻害効果を示さないことを発見した[32]。3新しいcucurbitane-type李氏らは発見されtriterpene saponins、11-O-MogrosideⅢ(11-oxomogrosideⅢ)、11-dehydroxymogrosideⅢと11-oxomogrosideⅣa・とcytotoxicityの結果12 Mogrosidesやあてはめられ、これらの3つの新しい化合物をはじめ結腸がん細胞線HCT-116と、がん細胞線SMMC-7721肝臓との境界ですこれら2つの肝がん細胞には明らかな細胞毒性は認められなかったが、より長い期間に依存する関係は、それらが細胞毒性である可能性を示している[8]。Matsumoto'sの研究によると、羅漢国抽出物はcyp1a1誘導を阻害し、ros産生を阻害し、それによって肝臓がんの発生を阻害することがわかった。これはおそらくahr活性の阻害によるものである[33]。weerawatanakornらは、モデルを確立するためにマウスの皮膚を刺激するためにtpa (12- o-テトラデカノイルホルボール13-アセテート)を用いた。その結果、によるmonascus机序は抽出inflammation-relatedを抑えるtumorigenesisとさまざまな信号経路条例にへばりつくように関連づけられて抑制核要因のupregulationをNF -кB[34]。
2.6消炎
panらは、リポ多糖(lps)によって活性化されたマウス生264.7マクロファージにおけるinosとcox-2の誘導性発現に対するluo han guo抽出物の阻害効果を調べた。その結果、ハン被告PI3Kと郭エキスを妨害する/ Akt / IKK・MAPK信号経路、核要因NFの活性化を抑えるκBdown-regulate遺伝子発現扇動的な要素をiNOS、マクロファージ[35]剤。chen yaoたちは、キシレンとカラギーナン誘発炎症実験を用いて、モグロシドの抗炎症効果を観察した。その結果、モグロシドはキシレンとカラギーナンによる炎症モデルに有意な影響を与えないことが示された[36]。しかし、diらは、モグロシドが主要な炎症遺伝子であるinos、cox-2、il-6を低下させ、parp1、bcl2l1、trp53、mapk9といった特定の炎症防御遺伝子を上昇させることによって、生の264.7細胞におけるリポ多糖(lps)による炎症を抑制することを発見した。同様に、●マウス穂はれモデル、Mogroside down-regulatesやIL-6 up-regulates PARP1の表現剤BCL2l1、TRP53、MAPK9と燃やす働きδ遺伝子に12-O-tetradecanoylphorbol-13-acetate炎症を誘導抑制し示唆Mogroside'の抗がんおよび抗糖尿病作用は、その抗炎症活性によって部分的に仲介されることがある[37]。Mogroside&か#39;sの抗糖尿病作用は、その抗炎症作用によって部分的に寄与しており、その関連するメカニズムは、さらなる調査と解明が必要である。
2.7その他の生物学的活動
wang qinたちは、モグロシドを用いて、正常マウスとシクロホスファミド(ctx)を抑制したマウスをgavageで治療し、マクロファージの貪食機能とt細胞増殖に対する影響を調べた。その結果、モグロシドは正常マウスの免疫機能には有意な影響を与えないが、ctx免疫抑制マウスのマクロファージの貪食機能とt細胞増殖を有意に改善することが示された[38]。zhao yanたちは、icrマウスに高脂肪食を与えて高脂血症動物モデルを確立した。モグロシドを一定量60日投与したマウスの平均血清tc値は86.07 mg/ dlで、高脂肪モデル群と比較して27.5%低下し、有意な効果を示しました(p<0.05)。tg含有量は44.5%減少した118.98 mg/ dlで、高脂肪モデル群よりも有意に低く(p<0.05)、平均hdl-c含有量は0.01 mg/ dlで27.3%増加し、有意なレベル(p<0.05)に達し、モグロシドが体内の脂質代謝を積極的に調節する生理機能を有していることを示唆した[39]。
さらに、ストレプトcoccus変異体はモグロシド培養液中ではほとんど増殖せずに増殖することから、モグロシドには抗虫歯効果があることが示唆された[40]。ある研究では、モグロシド抽出物の単回投与は、ヒスタミン誘導による鼻の擦りや引っかき行動に有意な効果を示さなかったが、300または1000 mg/kgのモグロシド抽出物は、4週間の連続摂食後に有意な阻害効果を示した[41]。chenらはmogrosideを発見した'sメインアグリコンモグロシド(mogrol)は、そのmogrosideことを示唆し、hepg2細胞におけるampkの強力な活性化因子である'sアグリコンモグロルは、少なくとも部分的にmogrosideに寄与するampkを、活性化させる&#in vivoでの抗高血糖および低脂血性効果[42]。

3展望
Currently, mogroside is mainly used as a new non-sugar, low-calorie sweetener。近年、動物レベルを中心に様々な生物活性が示唆されていますが、その作用機序は不明であり、細胞レベル、分子レベル、遺伝レベルでの詳細な研究に関する文献は多くありません。現代の薬理学や分子生物学の手法を用いて、モグロシドの生物活性のメカニズムをさらに研究することで、モグロシド機能性食品や医薬品前駆体の開発につながることが期待されます。また、体内のモグロシドの代謝経路および関連する代謝物に関する報告はほとんどありません。トリテルペン配糖体として、摂取後に胃腸消化酵素や腸内微生物叢によって分解されるのか、どのように分解されるのかは明らかではない。したがって、モグロシドの摂取後の生体内での形質転換、代謝経路、生成物、代謝機構を研究するためには、最新の分析技術とメタボロミクスを用いる必要がある。
参照
【1】張紅、李小紅。羅漢国の薬理作用と毒性に関する研究[j]。中国農業科学紀要,2011,27(5):430-433。
[2]張Liqin。低カロリー甘味料羅漢國サポニンの分離・解析・生物活性評価[d]。2004年、早稲田大学教授。
【3】居偉、程玉岩、張建。羅漢国研究の概要[j]。広西軽工業、2001年、4:4 -6。
【4】李デン鵬、張鴻瑞。羅漢国、広西の専門工場の研究と応用[j]。広西チワン族自治区の植物、2000,20(3):270-276。
[5] 金 J S、李 J Hにする。 Phytochemical and 薬理学的態様 of Siraitia grosvenorii羅應燦(ナ・ウンチャン) han 郭。東洋 薬学と実験医学[j]。2012年12(4):233-239。
[6] si j y, chen d h, tu g z .シライ酸f,新しいnor- Cucurbitacin と 小説 骨格から the 根 of Siraitia Grosvenorii [J]。 誌 of アジア 自然 製品 研究05シーズンまで、7(1):37-41た。
[7] li d, ikeda t, matsuoka n,et アルlo han kuo (siraitia grosvenori)の未熟果実から得られたククルビタン配糖体[j]。^「chemical and pharmaceutical bulletin,2006,54(10):1425-1428」。the new york times . 2018年3月25日閲覧。
[8] li d, ikeda t, nohara t,et al.ククルビタン配糖体from 生 果物 of Siraitia grosvenori[J]。 化学 2007年製薬公報55(7):1082-1086。
[9] li d p, el-aasr m, ikeda t,et アルsiraitia grosvenoriswingleの根から得られた2つの新しいククルビタン型糖鎖[j]。^「chemical and pharmaceutical bulletin,2009,57(8):870-872」。chemical and pharmaceutical bulletin(2009年). 2009年8月25日閲覧。
【10】張立琴,斉向陽。羅漢国サポニンと薬理活性に関する研究[j]。^『仙台市史』通史編、仙台市、2005年6月6日、22-24頁。
[11] chen w, wang j, qi x,らの抗酸化活性 自然 甘味料mogrosides、 果物 of Siraitia grosvenori [J]。^「international journal of food sciences and nutrition,2007, 58(7):548-556」。2007年3月15日閲覧。
[12]徐 Q、陳 S、邓 L et アル 抗酸化 モグロシドの効果に対して 酸化 ストレス induced by ヘキサデカン 酸 マウスのnit-1インスリン細胞で[j]。2013生物学の研究ははブラジル紀要医科46(11):949-955。
[13] xu qing, liang ronggan, su xiaojian, et al。健常者の血糖値と肝酵素活性に対する羅漢國甘サポニンの影響[j]。2007年(平成19年)3月28日:3 - 4号線を廃止。
[14] su xiaojian, xu qing, liang ronggan, et al。モグロシドの毒性作用に関する研究[j]。2005年(平成17年)3月26日:ダイヤ改正。
[15] qi xiangyang, chen weijun, song yunfei, et al。糖尿病マウスに対する羅漢國エキスの低血糖作用[j]。中国公衆衛生ジャーナル,2003,19(10):1226-1227。
[16] zhang liqin, qi xiangyang, chen weijun, et al。糖尿病マウスにおける血糖、血中脂質および抗酸化活性に対するモグロシド抽出物の影響[j]。中国薬理学会誌2006,22(2):237-240。
[17] suzuki ya, tomoda m, murata y,et al. antidiabetic effect 長露光の-term の with Siraitia grosvenori 自発的に糖尿病を発症した後藤柿崎ラット[j]。2007年British Journal of栄養97(4):770-775。
[18] qi x, chen w, liu l,et al.モグロシドを含むサイライティヤのグロブノーリエキスが型の細胞免疫系に与える影響 1 糖尿病 型 ネズミか[J]。分子 栄養&2006年≪食品研究、50(8):732-738。
[19] 鈴木 Y 村田、 Y、乾 H et al. siraitia grosvenoriのトリテルペン配糖体は、ラットの腸のマルターゼを阻害し、抑制する the 上昇 in blood glucose level 後 a シングル ラットにおけるマルトース経口投与[j]。農業・食品化学誌2005,53(8):2941-2946。
[20] qi x y, chen w j, zhang l q,et al.モグロシド抽出物 Siraitia grosvenori 準え 自由 radicals in 体外 を低下させたりといった 酸化 ストレス血清 グルコース→ lipid レベル アロキサンによって誘発された糖尿病マウスにおける[j]。栄養 2008年研究、28(4):278-284。
[21] wang q、xiao g .ラットにおけるモグロシドの慢性肝障害に対する保護効果に関する実験的研究[j]。2007年広西汉方薬30(5):54-56。
[22] xiao g, wang q .マウスの実験的肝障害に対するモグロシドの保護効果に関する研究[j]。中国の薬局,2008,19(3):163-165。
[23] liao changxiu, li shubo, xue qiang, et al。エタノール誘発性肝障害に対するモグロシドの拮抗作用[j]。2010年セ汉方薬、21(12):3116-3117。
[24] xiao g, chen z, li w, et al。ラットにおける四塩化炭素誘発性肝線維症に対するモグロシドの保護効果[j]。2012年(平成24年)4月1日:ダイヤ改正。
[25] wang q, wang w, long y, et al。肝星細胞hsc-t6および肝線維化関連遺伝子の増殖に対する羅漢国甘味抽出物の影響[j]。^『仙台市史』通史編4(通史編3)334 -334頁。
[26] xiao g, wang q .羅漢國甘味抽出物の肝保護効果に関する実験的研究[j]。2013年中国実験公式ジャーナル」、19(2):196-200。
[27] yao jiwei, tang hui, shen weihua, et al。羅漢國抽出物の用量を変えたマウスの生理機能への影響の観察[j]。遼寧省スポーツ科学技術,2007,29(3):24-26。
[28] yao jiwei, tang hui, zhou liang, et al。マウスを用いた羅漢國抽出物の運動耐久性および肝臓組織への抗酸化損傷に対する効果[j]。中国スポーツ医学誌,2008,27(2):221-223。
[29] yao j w, yang y l, tang h, et al。羅漢國エキスの訓練マウスの運動能力と心筋フリーラジカル代謝に対する影響[j]。北京体育大学ジャーナル2009,32(3):67-69。
[30]夏星、鐘鐘国、林采雲ら。モグロシドの抗疲労および低酸素耐性効果[j]。中国伝統医学実験研究会,2012,18(17):198-201。
[31]高崎 木嶋M T,村田 Y et al. Anticarcinogenic activity of natural 甘味料、cucurbitane glycosides Momordicaからgrosvenori[J]。2003年癌手紙198(1):37-42。
[32] mizushina y, akihisa t, hayakawa y,et al. structural analysis of Mogrol and its グリコシド阻害剤として 動物dnaポリメラーゼとヒトがん細胞増殖[j]。薬物のデザインで手紙&ディスカバリー2006年(平成18 3 (4):253-260
[33] matsumoto s, jin m, dewa y,et al.ジクロニルが促進する肝細胞増殖性病変に対するsiraitia grosvenorii抽出物の抑制効果[j]。^ a b c d e f g h『日本の歴史』第34巻第1号、109-118頁。
[34] WEERAWATANAKORN M、ヤン・ J Rで、蔡英文氏はこれ M L et アル抑制 effects of Momordica grosvenori マウス皮膚における12- o-テトラデカノイルホルボル13-アセトン酸誘発性皮膚炎症および腫瘍促進に関するswingle抽出物[j]。食品&機能、2014年。
[35] pan m h, yang j r, tsai m l,et al.抑制されたlps誘発によるmomordica grosvenori swingle抽出物の抗炎症効果 upregulation of iNOS and コックス2 in murineマクロファージか[J]。^『官報』第2152号、大正15年(1915年)12月15日。
[36] chen y, wang y, fan x, et al。モンクフルーツ甘味料の下剤および抗炎症作用に関する研究[j]。中国医薬学会誌,2011,27(3):202-204。
[37] di r, huang m t, ho ct . murine macrophagesにおけるmomordica grosvenori由来モグロシドの抗炎症活性food chemistry,2005,53(8):2941-2946。
[20] qi x y, chen w j, zhang l q,et al.モグロシド抽出物 Siraitia grosvenori 準え 自由 radicals in vitro を低下させたりといった oxidative ストレス血清 グルコース→ lipid levels アロキサンによって誘発された糖尿病マウスにおける[j]。栄養 2008年研究、28(4):278-284。
[21] wang q、xiao g .ラットにおけるモグロシドの慢性肝障害に対する保護効果に関する実験的研究[j]。2007年広西汉方薬30(5):54-56。
[22] xiao g, wang q .マウスの実験的肝障害に対するモグロシドの保護効果に関する研究[j]。中国の薬局,2008,19(3):163-165。
[23] liao changxiu, li shubo, xue qiang, et al。エタノール誘発性肝障害に対するモグロシドの拮抗作用[j]。2010年セ汉方薬、21(12):3116-3117。
[24] xiao g, chen z, li w, et al。ラットにおける四塩化炭素誘発性肝線維症に対するモグロシドの保護効果[j]。2012年(平成24年)4月1日:ダイヤ改正。
[25] wang q, wang w, long y, et al。肝星細胞hsc-t6および肝線維化関連遺伝子の増殖に対する羅漢国甘味抽出物の影響[j]。^『仙台市史』通史編4(通史編3)334 -334頁。
[26] xiao g, wang q .羅漢國甘味抽出物の肝保護効果に関する実験的研究[j]。2013年中国実験公式ジャーナル」、19(2):196-200。
[27] yao jiwei, tang hui, shen weihua, et al。羅漢國抽出物の用量を変えたマウスの生理機能への影響の観察[j]。遼寧省スポーツ科学技術,2007,29(3):24-26。
[28] yao jiwei, tang hui, zhou liang, et al。マウスを用いた羅漢國抽出物の運動耐久性および肝臓組織への抗酸化損傷に対する効果[j]。中国スポーツ医学誌,2008,27(2):221-223。
[29] yao j w, yang y l, tang h, et al。羅漢國エキスの訓練マウスの運動能力と心筋フリーラジカル代謝に対する影響[j]。北京体育大学ジャーナル2009,32(3):67-69。
[30]夏星、鐘鐘国、林采雲ら。モグロシドの抗疲労および低酸素耐性効果[j]。中国実験伝統医学研究会,2012,18(17):198-201.[31]高崎 木嶋M T,村田 Y et al. Anticarcinogenic activity of natural 甘味料、cucurbitane glycosides Momordicaからgrosvenori [J]。2003年癌手紙198(1):37-42。
[32] mizushina y, akihisa t, hayakawa y,et al. structural analysis of Mogrol and its グリコシド阻害剤として 動物dnaポリメラーゼとヒトがん細胞増殖[j]。薬物のデザインで手紙&ディスカバリー2006年(平成18 3 (4):253-260
[33] matsumoto s, jin m, dewa y,et al.ジクロニルが促進する肝細胞増殖性病変に対するsiraitia grosvenorii抽出物の抑制効果[j]。^ a b c d e f g h『日本の歴史』第34巻第1号、109-118頁。
[34] WEERAWATANAKORN M、ヤン・ J Rで、蔡英文氏はこれ M L et アル抑制 effects of Momordica grosvenori マウス皮膚における12- o-テトラデカノイルホルボル13-アセトン酸誘発性皮膚炎症および腫瘍促進に関するswingle抽出物[j]。食品&機能、2014年。
[35] pan m h, yang j r, tsai m l,et al.抑制されたlps誘発によるmomordica grosvenori swingle抽出物の抗炎症効果 upregulation of iNOS and コックス2 in murineマクロファージか[J]。^『官報』第2152号、大正15年(1915年)12月15日。
[36] chen y, wang y, fan x, et al。モンクフルーツ甘味料の下剤および抗炎症作用に関する研究[j]。中国医薬学会誌,2011,27(3):202-204。
[37] di r、huang m t、ho ct .マウスマクロファージにおけるモグロシドmomordica grosvenori由来の抗炎症活性[j]。2010年Bmc Syst Biol、4:141。
[42] gasch a p, werner washburne m .環境ストレスおよび飢餓に対する酵母の応答のゲノミクス[j]。ゲノム学Funct Integr危機以後、2:181-192てしまった。
[43] Vanz A L, Luensdorf H、アドナン 一、たち al. 生理反応。 of Pichia pastoris GS115 to メタノール-induced ハイレベル 生産 of the 肝炎 B 表面 抗原:catabolic adaptation,stress responses,and autophagic processes[j]。12 Microb細胞事実と11:103。
[44] Carnicer 10 M Pierick 、バン ダム J et al. 遺伝子組換えピヒア・パストリスの異なる酸素利用条件下におけるアミノ酸代謝の定量的メタボロミクス解析[j]。12 Microb細胞事実と11:83。
[45] dragosits m, stadlmann j, graf a,et al.展開したタンパク質に対する応答は、ピヒア・パストリスの浸透耐性に関与している[j]。2010年BMCゲノミクス、11:207。
[46] jorda j、jouhten p、camara e、et al. metabolic flux profiling of 组换え protein 分泌 Pichia pastoris 成長 ブドウ糖:・メタノール発刊[J]。12 Microb細胞事実と57。
[47] 」Sola」 A Jouhten P Maaheimo H et al. グリセロール/メタノール混合物を用いたピヒア・パストリスの代謝フラックス解析 chemostat 文化 at low and high 希釈 率 [J]。微生物学ローソクを消し153:281-290ますか。
[47] Jorda J、De イエス S s, peltier s,et al。 代謝磁束分析 of 组换え Pichia pastoris 成長 on 異なるグリセリン/メタノール 発刊 by 反復 試着 of 表示ポリオキサミド树脂-derived 13 c - データ from proteinogenic 網野 酸がか[J]。2014年新Biotechnol、31(1):120-132。
[49]メタノールを解明するためのピヒア・パストリスのunrean p .経路解析 代謝 and its 規制 for production 组换え性たん白質の[J]。2014年Biotechnolお父さん、30(1):28-37。
【50】関伯、金健、李華中。ピヒア・パストリスの外来タンパク質の分泌・発現能力の向上に関する研究[j]。2011年動物Microbiologica報、51(7):851-857。
[51]朱t、郭m、チワン族y、らの効果を理解する 外国 遺伝子 dosage on the 生理学 of Pichia pastoris by 主要遺伝子の転写解析[j]。^ a b c d e f g h i l l biotechnol, 2011,89(4):1127-1135。
[52] lin x q, liang s l, han s y,et al.定量的itraq lc-ms / msプロテオミクスは、異種タンパク質に対する細胞応答を明らかにする overexpression and the 規制 HAC1の in Pichia pastaris [J]。Jプロテオミクス、2013・91:58-72ある。
[53] liberek k、lewandowska a、zietkiewicz s . chaperones in control of protein disaggregation[j]。2008年EMBO J、27(2):328-335。


 英語
英語 フランス
フランス スペイン
スペイン ロシア
ロシア 韓国
韓国 日本
日本




