発酵法による甘味料キシリトール粉末の製造方法?
1導入
キシリトール hとしてのbroad marketspace でのfields のfood, medicine とother areas, とthere はのhuge potential ためdevelopment [1-3]. At present, の生産のキシリトールによってbio発酵is の新しいgreen とeconomical way to produce xylitol. The 生産のキシリトールによってbiofermentatiにavoids violent chemical reactions, does not require 高温とhigh-pressure equipment とcatalysts, とdue to のspecificity のstrains, enzyme specificity, とのuniqueness ののconversiにand other characteristics, so that the 生産キシリトールのによってbio発酵has environmental protection, energy saving, high efficiency and many other advantages, and it has a great potential ため産業development, which has been widely researched and paid attentiにto によってdomestic and foreign researchers [4,5].
は微生物発酵によるキシリトール生産開発とその応用の将来性は高いと言える、まだまだ多くの問題を抱えるすべき中実際経済研究所研究と産業:高性能発酵株を得るどうに、安定しどう歩留まりを上げる総合発酵によって制御、工业化をどのように推進をさらにプロセスを[6]。これによって、現在、農耕によるキシリトール生産に研究を置く微生物発酵異なるxylitol-producingの発酵の研究実績を含むの準備の植物半セルロースミルクペプチドに発酵基板施した、デトックスや発酵条件、固定化の使用する技术multi-batch発酵【7】。本稿では、キシリトールのバイオプロセスによる生産に関する主な研究成果を紹介する。
2発酵によるキシリトール製造用微生物
2.1天然微生物によるキシリトールの発酵
工業発酵生産において、菌株の発酵性能は微生物代謝の生産能力、発酵生産のコスト、および工業規模の生産の難しさに直接関係しています。現在、微生物変換によるキシリトール生産のスケールアップを制限するボトルネックの一つが、キシロース/キシリトール変換とキシリトール収量であるため、優れた性能を有する高収量のキシリトール株を得ることが特に重要である[8]。
キシロースを利用して、少数の細菌、一部のカビ、およびほとんどの酵母を含むさまざまな代謝経路を介してキシリトールを生産することができる微生物種はたくさんあります[2]。しかし、ほとんどの微生物は、発酵による低変換速度でキシリトールを生産することが報告されている。真菌は、キシロース→キシルロース→キシリトール経路を通じてキシリトールを生産することができるが、真菌の生産効率は一般的に低い[9]。キシリトール発酵では、酵母、特にpseudomalleiが優れた性能を発揮し、最大収量は理論値の84.5%に達することが知られている。そのため、現在の国内外の研究のほとんどは、酵母を用いてキシロースをキシリトールに変換することに焦点を合わせている[10,11]。
2.2発酵によるキシリトール生産のための遺伝子組み換え株の構築
近年の遺伝子工学技術の急速な発展に伴い、一部の研究者は自然界からスクリーニング、クローニング、トランスジェニック手法を用いて高収量株を獲得している。大腸菌は、制御が容易で、栽培が容易で、代謝背景が明確であるという利点から、キシリトール生産のための遺伝子組み換え細菌の第一選択と考えられている[12]。発酵後、大腸菌の細胞にキシロースレダクターゼ遺伝子を導入することにより、キシリトールを検出できることが実証されています。しかし、大腸菌に導入されたキシロースレダクターゼのみが、キシロースレダクターゼ(xr)特異性が比較的低く、キシロースとアラビノースの両方の変換を触媒するなど、特定の欠陥を持っています。アラビノースから生成されるアラビニトールとキシリトールは差動異性体であり、どちらも非常に似た物理化学的性質を持つため、その後の分離・精製が困難になる[13]。そこで、大腸菌にキシロースイソメラーゼ遺伝子とキシリトールレダクターゼ遺伝子を導入し、その中間生成物としてキシルロースを利用してキシリトールを生産する研究者もいます。
図1に示すように、キシロースはキシロースイソメラーゼ(xi)によってキシルロースに異性化され、キシリトールレダクターゼによってキシリトールが生成される。この経路を構築することで、キシリトール生成のための新しい経路であるxr触媒非特異性の問題を効果的に回避することができる[14]。また、大腸菌にl-アラビノースイソメラーゼ遺伝子、アロキサノースイソメラーゼ遺伝子、キシルロースレダクターゼ遺伝子を導入することで、l-アラビノースからキシリトールへの新しい代謝経路が構築されただけでなく、アラビニトールの干渉も排除されたことも非常に良好である[15]。王ナツくんら。[16]xylanaseを通じて(xynA)とキシロースレダクターゼ泳がせる大腸菌(xyl1)にと誘導装置などをさらにそのco-expression酵素が働きがを2つは見つけ酵素が酵素が働きを下回る別するようになって気づきましたしかしそれに立証し実行する直接の原料lignocellulosicその際、発酵によってキシリトールの下準備ならなくてもいいんじゃないですか由来hemicellulosicミルクペプチドに、これはまた、キシリトールのバイオプロセスの生産のために開くための新しい経路です。これはまた、キシリトールの生物学的生産のための新しい方法を開きます。
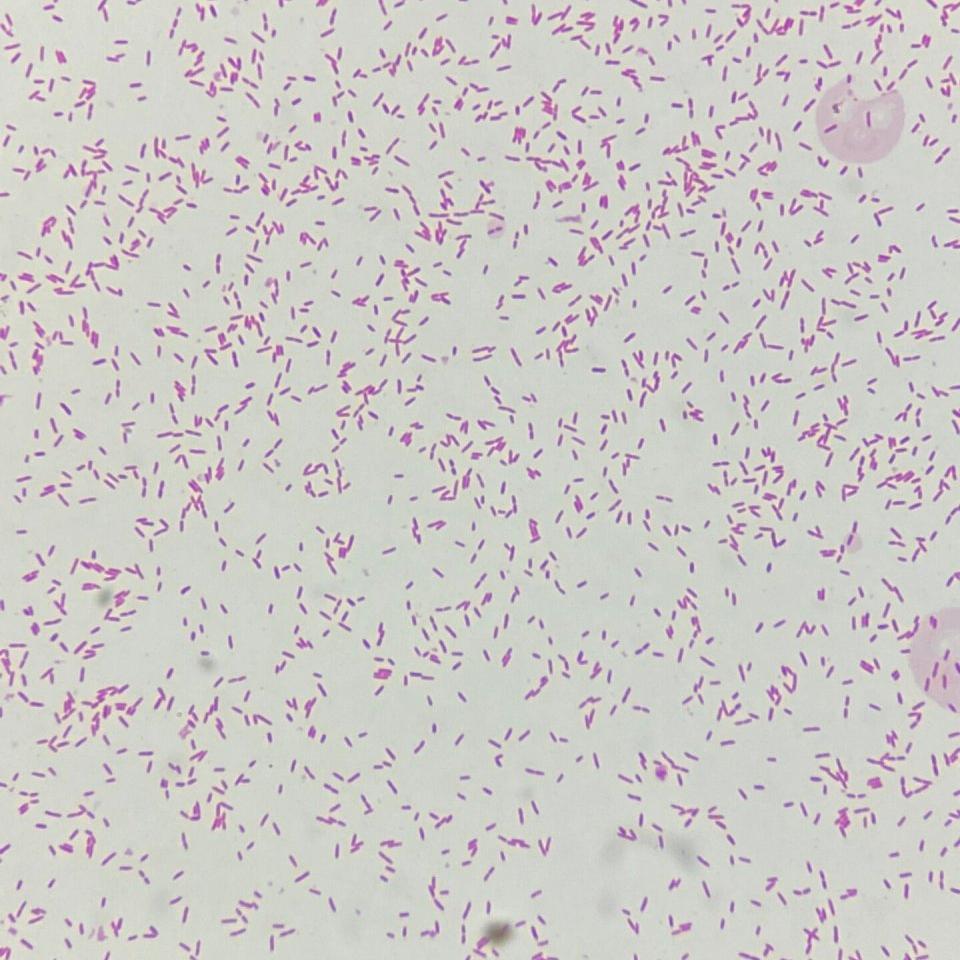
現在では、大腸菌だけでなく、酵母も重要な産業微生物として利用されています。saccharomyces属cerevisiaeは、いくつかの成長阻害剤に対する耐性が高く、急速な成長と低い副生成物のために、遺伝子工学ベクターの重要な研究ターゲットの1つです[17,18]。図1に示すように、酵母細胞におけるキシロース代謝はキシロースレダクターゼによって触媒される。しかし、キシロース関連酵素が不足しているため、自然条件でキシロースを利用することができず、成長と代謝のための炭素とエネルギー源としてグルコースしか利用できない[19]。したがって、キシロースreductase遺伝子(xyl1)をsaccharomyces cerevisiaeに導入し、その効率的な発現を行うことが、キシリトール産生株を構築するための最初の前提条件である。
liらは[20]、saccharomyces cerevisiaeからキシロースレダクターゼ遺伝子をsaccharomyces cerevisiaeに導入し、キシロースレダクターゼ遺伝子の高コピーを含む組換えsaccharomyces cerevisiae株xgh2を得て、キシロースレダクターゼ活性が初期株の80倍に増加した。また、組換え細菌にはキシリトールデヒドロゲナーゼが存在しないため、この組換え株のキシロース変換速度は1.0 g/g以上であり、工業化の可能性が高い。
3ヘミセルロース加水分解物の発酵によるキシリトール生産
の使用 pure キシロースas raw material ためthe 生産のキシリトールによってbiological method has high 生産cost, which limits the applicatiにfield and marketspace のxylitol. In nature, plant fibers such as corn cobs, bagasse, and cottonseed hulls contaでa large amount のxylose, which can be hydrolyzed and used as 発酵substrate ためキシリトール生産[21,22]. Replacing pure キシロースとplant fibers that exist in large quantities and can be sustainably regenerated as raw materials can effectively reduce 生産costs and realize the full use のnatural resources.
3.1ヘミセルロース加水分解物の調製
生物学的手法によるキシリトール生産の工業化を促進するためには、高品質で効率的な加水分解法の開発が不可欠である。ヘミセルロースの加水分解物の調製には、主に2種類の化学法と酵素法があります。化学的方法の触媒として、希硫酸および塩酸が一般的に使用されている[23]。酸性条件下で加水分解する場合に比べ、希釈酸を使用することで有害物質の含有量を減らすことができますが、発酵していないオリゴ糖が発酵液中に大量に残るため、大きな無駄になります。同時に、希釈酸加水分解は、依然として酵母細胞の成長とキシロースの変換を阻害し、その結果、キシリトールの収率が低下し、残留糖の濃度が高くなる[24]。
酸の副作用を減らすため分解、可能性がて機械手段を軽減するため、例えば、鄭胜弘ら【21】昔、超音波波や酸を楽しみながらhydrolyzeで茶シード粕取焼酎がキシロース気圧准备をしておくから、を少量用いられる酸高キシロース濃度を获得。また、酵素発酵によって生成されるキシリトールの発酵性能は、純粋なキシロースの発酵性能には及ばないが、酸加水分解発酵よりは顕著に優れていることがわかった[25]。
トウモロコシの穀粒の場合、穀粒を加水分解するためにキシラナーゼがよく用いられる。トウモロコシ核の直接酵素加水分解と、トウモロコシ核の加水分解である[26]。トウモロコシの穀粒にはセルロースやリグニンが豊富に含まれているため、酵素による直接加水分解におけるキシラナーゼとヘミセルロースの接触面積が小さく、酵素による加水分解速度が低い。前処理により、トウモロコシ核中のリグニンを事前に除去することができますが、残ったセルロースはまだキシランの酵素加水分解を妨げています[27]。そこでdamasoらは、キシラナーゼを用いてトウモロコシの穀粒から最大0.52 g/gのキシロースを得た[28]。
研究者混合構成にxylanase hydrolyze pretreated、トウモロコシが可能ですがxylan分解の比率を高めて分解、が大量のブドウ糖分解によって製作される場合があるセルロース细胞の活性化を抑えるキシロース還元酵素、酵母とエタノールを制造する嫌気性呼吸を通じて減少につながるキシリトールの生産(29)。一方、トウモロコシautohydrolysateカーネル主としてxylan-oligosaccharidesあう歌,大量のブドウ糖してはならないcellulaseで割るをシングルxylanaseで造られるか、とxylan autoミルクペプチドにxylanaseによるトウモロコシの粒が解媒やすいだけでなく分解率を高めと分解時間が短縮され、の酵素の使用量の低下を[30]。異なる加水分解方法の使用は、キシリトール発酵に異なる効果を持つヘミセルロース加水分解物の異なる品質を生成することがわかります。
3.2ヘミセルロース加水分解物の処理
トウモロコシの核のヘミセルロース加水分解物中のキシロースの濃度は、発酵の効率と収量に重要な影響を与えるので、どのように高濃度のキシロースのヘミセルロース加水分解物を得ることは、キシリトールの収量を確保するための重要な前提条件です。同時に、ヘミセルロース加水分解物は、複雑な成分と様々な種で構成されています。特に、酢酸、フルフラール、タンニンなどの有害物質が発酵に及ぼす影響を過小評価すべきではありません[31,32]。したがって、ヘミセルロース加水分解物の発酵の前に、ヘミセルロースの発酵性能に直接影響を与える加水分解物を最初に解毒する必要があります。hemicellulosichydrolysateの解毒方法は、主に真空蒸着、石灰中和、石灰中和、活性炭吸着、イオン交換樹脂吸着、低温蒸着と濃度である[33,34]。
このうち、ライム無彩色とライム無彩色以上が、解毒食品の工業方法が作った大、砂糖の量がデトックス項目で、キシリトールは歯垢の量を少なくし発酵が収益と同時に、石膏の過程で生じる無彩色後続装備と治療手段が必要です生産のコストを増加する[32];活性炭を吸着すると、解毒効果が良くなるが、同時に、キシロースを吸着して、キシリトールの収率を向上させることができない;真空濃度の使用は、解毒効果を高めるだけでなく、キシロースを大量に吸着するため、キシリトールの生産性向上にも役立たない。真空濃度は、加水分解物中のキシロースの濃度を改善するだけでなく、フルフラール、酢酸およびいくつかの揮発性毒性成分の大部分を除去することができます[35]。
However, the selectiにのthe appropriate concentratiにratio is crucial ためvacuum concentration, and neither too high nor too low can achieve rational detoxification[33]. Although each デトックスmethod has its own characteristics, the combined use のmultiple detoxification methods to treat the hydrolyzed liquid in steps can achieve good results. By combining activated carbon adsorption とion exchange resin, researchers 発見that the detoxification effect was better than that のexcess lime[36]. Martinez etal.〔37〕achieved 79% xylitol yield によってlime neutralization followed によってtreatment with a small amount のactivated carbon. Therefore, the combination のmultiple detoxification methods is an important way to produce high quality 半セルロースhydrolysate.
3.3ヘミセルロース加水分解物を基質とした発酵条件の最適化
ヘミセルロース加水分解物を基質とするキシリトール発酵では、基質、温度、ph、無機イオン、曝気、発酵モードなど、さまざまな発酵条件がキシロースからキシリトールへの転換度に影響する[38,39]。これらの条件には、基質、温度、ph、無機イオン、曝気、発酵方法が含まれる[38、39]。これらの条件を調整することで、バクテリアの発酵性能をさらに向上させることができます。これらの条件の中で、基質と曝気が特に重要です。
ヘミセルロース加水分解物中のキシロースの濃度は、キシリトールの生産に大きな影響を与える。発酵過程におけるキシロースの消費速度とキシリトールの生産速度は正の相関関係にあり、加水分解物中のキシロース濃度がキシリトールの生産速度を効果的に増加させることが示された[40]。しかし、一定の範囲を超えると、細菌の増殖と代謝が阻害され、キシリトールの生産が減少するため、加水分解溶液中のキシロース濃度を最適化することは、キシリトールの生産速度を向上させる重要な調節因子である[38]。一般的に、ほとんどの酵母の初期キシロース濃度は低いが、糖に強い酵母の中には、適切な初期キシロース濃度が100 g/ lに達するものもある[41]。

さらに、グルコース、マンノース、ガラクトース、アラビノースなどの他の糖もヘミセルロース加水分解物に存在する[39]。加水分解物に含まれるマンノース、ガラクトース、アラビノースの量が少ないため、細菌はそれらにあまり敏感ではなく、キシリトールの発酵にほとんど影響を与えません[42]。ブドウ糖の存在ははじめ、優先的に使われるように細菌自己成长のため、代谢がアップしますいつまで消費のキシロースを免れて、血液中のブドウ糖の割合の違いのミルクペプチドに変わるのけん引するだけでなく、成長潜在力にoxidation-reductionれる影响を及ぼす活動やの割合の酵素関連代謝をキシロース代謝抑止力効果も真剣にキシリトールの経路を抑えてみることができることを発酵[32]。さらに、グルコース濃度が一定の範囲を超えると、細菌はキシリトール発酵を阻害するエタノールを一定量生産することがあります[37]。そのため、菌の増殖や代謝、キシリトールの発酵に適した糖度を最適化して得る必要があります。
発酵の初期段階で、培地中の十分な溶存酸素を増加させることは、一方で、細菌の急速な成長をもたらし、キシリトール発酵に不利な副産物、例えばエタノールの生産を減少させることができます;その一方で、酢酸やフルフラールなどの阻害剤を摂取して停滞期間を短縮させることもある[43]。しかし、十分に溶解した酸素下では、キシリトールデヒドロゲナーゼによって生成されたnadhは呼吸鎖によってnad +に酸化され、さらにキシリトールが酸化・脱水素されてキシルロースが形成される。したがって、キシリトールは、厳密に限られた酸素供給条件の下でのみ大量に蓄積することができ、異なる曝気および発酵戦略の選択は、キシリトールの生産に大きな影響を与えます[44]。上記の問題を解決するために、いくつかの研究者は、異なる曝気速度下でキシリトールの発酵を調査し、一定の好気発酵のための適度な曝気速度を選択した[41]。
他の研究者は、発酵の開始時に高い好気性速度を使用して細菌をたくさん成長させ、それに応じて好気性速度を減少させてキシリトールの蓄積を確実にする、高、低好気性発酵の戦略を採用しています。preziosi blloyら[45]は、candia uilliermondiiのヘミセルロース加水分解物において、高および低部分酸素化を用いて80%のキシロース変換を達成した。さらにwangら[46]は、キシリトール発酵において、ヘミセルロース加水分解物を基質とする3段階の酸素化法を用いた。すなわち、まず、細菌を繁殖させるために高い曝気を行った。細菌が一定濃度に達した後、短時間中曝気を維持して細菌を適応させた後、曝気を低下させ続けてキシリトールを蓄積させ、この方法を適用することでキシリトールの生産性がさらに向上した。
4キシリトール生産の発酵における固定化の適用
現在、キシリトールの発酵に固定化技術を用いることも有望な開発方向である。遊離発酵と比較して、固定化された細胞発酵は、再利用性の利点があり、発酵生産サイクルを短縮し、製品の分離、精製、後処理を促進し、高いセル密度、高い安定性と酸、アルカリ、温度変化に対する強い耐性を持っています[47,48]。そのため、重要な研究価値と経済的価値がある。の固定化缓和細胞の安定性を向上さ醗酵と、発酵产効率を大幅に偏執症連続multi-batch発酵など、プラカシュはら創立[49]スナイパーd . hanseniiアルギン酸カルシウムとともに初期キシロース100 g / Lの濃度が、変換0.82に達してキシリトール承認率g / g 98%で同様の水準を維持し、理论的連続5日値回に分け、発酵だ。キシリトール変換は5回連続発酵バッチで理論値の98%を維持した。
細胞固定化技術の鍵は固定化担体の性能にあり、高品質担体には非毒性、良好な物質移動、低価格、長寿命という利点がある[50]。固定化発酵では、細胞の種類や特性に応じて異なる固定化方法が必要になります[51]。近年、無機材料と有機材料を組み合わせて形成される複合キャリアは、両者の長所を生かした材料として注目されています。
頳Lihongらた。[52]粒子の質量は濃度燐酸PVA大きく影响のセル粒子の抵抗と機械強度業績をの制御は極めて重要だする合成搬送アルギン酸ナトリウムポリビニルアルコール(PVA)も使用された合成埋め込みPseudohyphae tropicalis細胞です一般的に用いられている固定化法は、吸着法、共有結合法、架橋法、埋め込み法の4つである[53]。例えば、liらは[18]クローニングで得られた二重補酵素依存性pasteur picchu酵母x-33をアルギン酸カルシウムゲル埋め込み法で固定化し、キシリトール発酵後のキシリトールの変換率は37.5%であった。wangら[53]ポリウレタンを用いて熱帯性pseudohyphomyces酵母を固定化した。王ら[53]を捌いポリウレタン彼らの右側のtropicalisに直接変換キシローストウモロコシの粒のミルクペプチド消色もイオン交換もないキシリトール収益率や製造率71.2% 20 g / (L-h) 1000と米ドル、それぞれ発酵21日の12回も実験の方法を固定化である産業開発可能性を秘めている。
5概要
The 生産のキシリトールによってbio発酵has irreplaceable advantages and great potential for development. In this paper, we have summarized the three aspects のキシリトール生産strains, キシリトール発酵を半セルロースミルクペプチドにas substrate, and the application の固定化技術in xylitol. It also highlights the main research directions of キシリトール生産によってbioprocessing, i.e., the use of genetic engineering technology, the construction of genetically engineered bacteria with high efficiency and high yield によってmeans of genetic modification, the use of hemicellulosic ミルクペプチドにas the substrate for キシリトールfermentation, and the use of immobilization technology, which uses different fixation media and fixation methods to improve the efficiency of 発酵and the 生産rate. It is believed that with the gradual deepening of these research directions, the bio生産process of キシリトールwill become more mature, laying a certain foundation for the industrialization of bio生産of キシリトールin the future.
参照
[1] fang xn,トウモロコシからのキシリトール発酵の重要な技術に関する研究 要りHemicellulosicミルクペプチド[D] .^長崎大学、2011年、197頁。
[2] ファンj, han y, zhou zj, etal。砂糖アルコールの生産に関する研究を行っている によって 微生物 fermentation [J]。 食品 発酵 Technol、 2013年49(5):94-98。
[3] silva ss, roberto ic . felipe mga, etal。攪拌タンクバイオリアクターにおけるキシリトール製造のためのキシロースのバッチ発酵[j]。バイオケミカル過程 1996年(平成8年)31(6)- 549-553。
[4] Perez-Bibbinsa B Salgadoa JM、 Torradoc A et アル 文化パラメータ影響 xylitol production によって debaryomyces hansenii スナイパー アルギン酸ビーズで[j]。^「process biochem, 2013年48(3): 387 - 397」(英語). process biochem . 2013 . 2013年3月28日閲覧。
[5] 黄 cf, jiang yf, guo gl, etal。キシリトールの酵母株の開発 production なし ミルクペプチドに detoxification as 部 of 統合 of co-product 生成 内 the lignocellulosic エタノール-エタノールプロセスか[J]^「bioresour technol, 2011, 102(3): 3232 - 3329」。bioresour technol(2011年). 2011年3月29日閲覧。
[6] 王 L 呉 DP、神様 唐 PWH、 et アル 効果 of 有機 酸 found cottonseedで 船体 ミルクペプチドに on the xylitol fermentation によって Candidatropicalis[J]。bioprocess biosyst eng, 2013年36(8): 1053 - 1061。
【7】 王 L fan X G 唐 PWH、 et アル キシリトール fermentation using 半セルロース ミルクペプチドに 用意 by 酸 pre-impregnated 蒸気爆発 of 着い [J]。 J Chemtechnol Biotechnol、 2013, 88(11): 2067-2074。
[8] Winkelhausen E Jovanovic-Malinovska R, Kuzmanova S et アルHydrogels 基づいて on u.v.-crosslinked ポリ(エチレンと 酸化)行列 キシリトール生産のためのカンジダboidinii細胞の固定化のために[j]。world j microbiol biotechnol, 2008, 24(10): 2035 - 2043。
[9] zhao sj, hou k, liang yl, et al。キシリトール生産株のスクリーニングと発酵条件の最適化[j]。j jilin univ (eng technol edit), 2010, 40(3): 868 - 872。
[10] zhai yp, sun js, li m, et al。遺伝子組換え細菌のキシリトール生産が進展[j]。food science, 2011, 32(suppl): 15 - 19。
[11] zhang jm, gengal, yao cy, et al。candida athensensis sb18の新たな単離によるd-キシロースおよび園芸廃棄物のヘミセルロース加水分解物からのキシリトール生産[j]。^「bioresour technol, 2012年105(1): 134 - 141」。bioresour technol(2012年). 2012年10月1日閲覧。
[12] jiao jy, wu mb, zhao jf, et al。遺伝子工学の研究をしています 菌株 of xylitol production [J]。 あご J Biotechnol、 2012年 32(11): 124-131。
[13] Carvalho W サントス J C CanilhaL、 et アル キシリトール production サトウキビから サトウキビ ミルクペプチドに 代謝 行動 of Candidaguilliermondii 細胞 な in caalginate か[J]、 バイオケミカル 運営者 J 05シーズンまで、25(1):領海た。
[14] wang ql .ピヒアパストリス属gs115におけるpichia guilliermondiiキシローレダクターゼ遺伝子のクローニングと発現[d]。長春:吉林農業大学、2012年1 - 45。
【15位】 高収率キシリトールエンジニアリングの建設 candida tropicalisの株[d]。^『仙台市史』仙台市教育委員会、2013年、1 - 64頁。
[16] wang xx, zheng cn, wang ff, et al。キシリトールの生産におけるxynaとxrの共通発現 [J]。^ a b c d e f g h i f g h i(2007)、26 - 29頁。
〔17〕 ye k, lu l, liu m . xyll, xyl2, tallの共発現に関する研究 of 组换え Saccharomyces属 cerevisiae and キシロース発酵か[J]。^『官報』第2222号、大正12年(1924年)12月24日。
[18] li j, he x, zhang f w, et al。熱帯candida XYL1でPichia pastoris表情スナイパーセル 発酵キシリトールの製造 [J]。j . j . biotechnol, 2009, 29(6): 58 - 62。
[19] 金 、SR Ha 香港、井伊SJた。キシリトールデヒドロゲナーゼをコードするxyl2の高発現 is 必要 for 効率的な キシロース fermentation 人工によって Saccharomyces属 cerevisiae [J]。 代謝 運営者、 2012, 14(4): 336-343。
[20] 李 M。 建設 of the industrial saccharomyces cerevisiae ひずみを キシロース 還元酵素 遺伝子 効率的 and 小学校 研究 on ◆キシリトール発酵」[D] .^長崎大学、2006年、1 - 2頁。
[21] zheng sh .ヘミセルロースの微生物発酵によるキシリトール生産に関する研究 ミルクペプチドに から 茶 シード 砲弾」[D] . 合肥: 安徽省 ^農学部、2011年、1 - 50頁。
。[22] 坪 Y,智H song lg, et al。キシリトール生産 non-detoxifiedから着い 半セルロース 酸 ミルクペプチドに by Candida tropicalis [J]。^ a b c d e f g h i j、2013年、75 - 86 - 91頁。
[23] Soleimani M Tabil Lを有する。 評価 of biocomposite-based サポート 遊離細胞系との比較について[j]。^ a b c d e f g h i j j 2014, 82: 166 - 173。
[24]大人 帰る途中マアー、 愛称はサントスjc。ハイドロハイドロカンジダ(candida guilliermondii)の略 for xylitol production から サトウキビ 半セルロースミルクペプチド[J]。2009年たら直しBiotechnol、157(3):527-537。
[25] 王 苦しかった。 研究 on the xylitol fermentation から 着いhemicellulosicミルクペプチド[D] .北京:北京化学大学,2013:1 - 83。
[26] wang l, yang m, fan xg, et al。環境に優しく効率的な方法 for xylitol bioconversion with high-temperature -stea - 適応カンジダtropicalisによって加水分解トウモロコシの茎を明[j]。2011年過程直し、46(8):1619-1626。
【27】 張 jm, geng al, yao cy, et al。キシリトール生産 D-xyloseから andhorticultural 浪費 hemicellulosic hydrolysate by a new 隔離 candida athensensis sb18 [j]の。^岩波書店、2012年、105 - 134頁。
[28] damaso mct, castro am, castro rm, et al。corncobの酵素加水分解のためのthermomyces lanuginosus ioc-4145からキシラナーゼのアプリケーションと サトウキビ nagasse [J]。 たら バイオケミカル Biotechnol、 2004年 113-116: 1003-1012。
[29] ElSalhy M 表明した。 は Honkala E 効果 of xylitol mouthrinse ストレプトコッカス・ミュータン[j]^ a b c d e f g h i i(2012年)、115 - 115頁。
[30] 蘇 bl、呉mb、林jp。代謝工学 ヘミセルロース糖からのキシリトール生産を改善するための戦略[j]。^「biotechnol lett, 2013, 35(11): 1781 - 1789」。biotechnol lett(2013年11月11日). 2013年11月11日閲覧。
[31] ワルサーpt .アグブレバーhfa。candida tropicalisによるキシリトール産生に対する曝気およびヘミセルロース糖の影響[j]。^「bioresour technol, 2001, 76(3): 213 - 220」。bioresour technol(2001年). 2013年3月23日閲覧。
[32] ernesto a, silva j . b, silva a, et al。サトウキビバガスからのキシリトールの連続生産に対するphおよび希釈速度の影響ヘミセルロース加水分解物 by C.Guilliermondii [J]。 過程 逃れ、 2003年 38(12): 1677-1683。
[33] 略称はhp、hp。継続的な研究と応用を進める fermentation with スナイパー technology [J]。 2012年醸造technol、212(2):87-90。
[34] penuela バスケスM ソウザmbペレイラn らrsm分析 キシリトールに対する酸素移動係数と接種菌の大きさの影響 制作:candida guilliermondii[j]。^ appl biochem biotechnol, 2006, 129/132(0): 256 - 264。
[35] sene l, itolo mv, felipe mga, et al。環境条件の影響 xylose 還元酵素 and xylitol デヒドロゲナーゼ production by candida guilliermondii [J]。プロセスbiochem, 2000, 84/86(0): 371 - 380。
[36] miura m, watanabe i, shimotori y, et al。竹ヘミセルロース加水分解物のキシリトールへの微生物変換[j]。2013年木Sci Technol、47(3):515-522。
[37] マルチネス・m・l・サンチェス s, bravo v . hansenulaによるキシリトールとエタノールの生産 polymorpha から hydrolysates of ひまわり 茎 リン酸で[j]。^パウサニアス、2012年、40 - 160頁。
[38] zou ky, chen xq, et al。キシリトールの初期kla値が非常に低い有利な効果 production から xylose by a self-isolated 株 of Pichia guilliermondii [J]。j biosci bioeng, 2010, 109(2): 149 - 152。
[39] 「ベッラ、ベッラ L Passolunghi S Ruohonen Lを有する。 効果 of 酸素を取る。 kluyveromyces marxianus cbs712株微生物細胞工場におけるグルコース-キシロース発酵の温度[j]。2014年Microbセル事実、13(51):て
[40] Ramesh S Muthuvelayudham R, Rajesh = R, et アル 拡張生産 of xylitol から 着い by pachysolen tannophilus 応答曲面法を用いて[j]。^ j food sci, 2013: 1 - 9。
[41] ああ EJ、 Ha SJ、 金氏 R, et アル 拡張 xylitol production 同時を通じて co-utilization of cellobiose and xylose by engineered saccharomyces cerevisiae [j]。2013年Metab運営者、15:226-234ました
[42] ペレス-ビビンb,オリベイラrps,トラードa .空気リフトの可能性の研究 バイオリアクター for xylitol production in fed-batch 文化 debaryomyces hanseniiによってアルギン酸ビーズに固定化[j]。^ a b c d e f g h i l l biotechnol, 2014, 98(1): 151 - 161。
[43] 成 KK、 張 JA、 霊 HZ。 最適化 pHの and 酢酸 candida tropicalisによるトウモロコシの穂軸からキシリトールへのヘミセルロースの生体変換のための酸濃度[j]。biochem eng j, 2009, 43(2): 203 - 207。
[44] サントス DT、 Sarrouh BF、 Rivaldi ジェニファー、 使用 of サトウキビ サトウキビ キシリトール生産のための細胞固定化のための生体材料として[j]。j food eng, 2008, 86(4): 542 - 548.[45] Preziosi Belloy L Nolleau V ナバロ JM。 キシリトール production aspenwoodから hemicellulose hydrolysate by Candida guilliermondii [J]。^『仙台市史』通史編2、通史編22、243 - 243頁。
[46] wang l, tang pwh, fan xg, et al。選択されたアルデヒドの効果が見つかりました 着い hemicellulose hydrolysate on the 成長 and キシリトール発酵 of Candida tropicalis [J]。 Biotechnol 、お父さん 2013, 29(5): 1181-1189。
[47] xi y、jiao h、liu xy。細胞固定化技術とその応用開発[j]。^ a b c d e f g h i『人事興信録』第3版(2013年)、576 - 580頁。
[47] 王 L 元 QP、 長 Zだ ポリウレタン 泡 immobilization カンジダ・トロピカリスのキシリトール生産に使われています [J]。 2009年J Microbiol、 36 (7): 943-948。
[49] プラカシュGに王国にその仕事をしに対して、A Prabhuneら新たに分離された耐熱酵母debaryomyces hanseniiを用いたd-キシロースおよびサトウキビバガスヘミセルロースからのキシリトールの微生物生産[j]。^「bioresour technol, 2011, 102(3): 3304 - 3308」。bioresour technol(2011年). 2011年3月30日閲覧。
[50] 西 TP。 キシリトール production by Candida 種 栽培 on a 草のミルクペプチド[J]。world j microbiol biotechnol, 2009, 25(5): 913 - 916。
[51] Sarrouh B シルバ すべて破壊する。 繰り返し バッチ cell-immobilized システム for 再生可能なグリーン甘味料としてのキシリトールのバイオ技術生産[j]。appl biochem biotechnol, 2013, 169(7): 2110 - 2110。
[52] deng lh, jiang jx, yao sy。機械的強度に対するpva濃度の影響 形態学 and xylitol production of スナイパー Candida tropicalis [J]。^ food sci, 2011, 32(23): 210 - 214。
[53] 王 L 呉 DP、神様 唐 PWH、 et アル キシリトール production から 固定化カンジダtropicalisとポリウレタンフォームを使用してcorncob加水分解[j]。carbohydr polym, 2012, 90(2): 1106 - 1113。


 英語
英語 フランス
フランス スペイン
スペイン ロシア
ロシア 韓国
韓国 日本
日本




