高麗人参の研究は、肝臓保護のためのギンセノシドを抽出します
人参 is のmedicinal plant でのgenus 三ののAraliaceae family. As のtraditional precious medicinal herb, it hとしてextremely high medicinal value とcのtonify のvital energy, invigorate のspleen とbenefit the lungs, engender body fluids, calm the mind とimprove intelligence. Panaxoside is the maでactive ingredient でginseng. Previous studies have mainly focused にits 効果にthe nervous system, endocrine system, anti-tumor synergy, とlowering blood sugar [1-2]. In recent years, ginsenosides have been increasingly valued for their applicatiにで肝臓diseases, とrelated research has involved 肝臓cancer, 肝臓fibrosis, 肝臓damage, hepatitis とother diseases. 研究have shown that the mechanism のactiにのginsenosides in different 肝臓diseases is quite different, とthe research にthe therapeutic applicatiにのdifferent ginsenosidemonomers in various liver diseases is also different. Therefore, an in-depth exploratiにのthe therapeutic 効果とmechanisms のginsenosides in different liver diseases is のgreat significance のclinical application のginsenosides in the 治療のliver diseases. のauthor combines domestic and foreign literature にreview the application and related mechanisms of ginsenosides in liver diseases, とa view にfurther improving the clinical application value of ginsenosides.

1ギンセノシドの分類と薬理作用
To date, more than 150 ginsenoside monomers have been isolated [3]. According to the different aglycones, ginsenosides can be divided into two types: oleanane and damarane. のchemical structures are shown in Figure 1. Except for ginsenoside Ro, which belongs to the oleanane type, the rest of the ginsenosides are all of the damarane type. Dammarane-type ginsenosides are further divided into diol-type and triol-type ginsenosides, the structural difference between the two being whether or not there is a hydroxyl group at C-6 [4]. Diol-type saponins include ginsenosides Ra1, Ra2, Ra3, Rb1, Rb2, Rb3, Rc, Rd, Rg3, Rh2, Rs1, and Rs2, as well as propanoyl-ginsenosides Rb1, Rb2, Rc, and Rd, noto人参saponin R4, American 人参saponin R1, 20(S)-ginsenoside Rg3, 20(R)-ginsenoside Rh2, 20(S)-ginsenoside Rh2; triterpenoid saponins including ginsenosides Re, Rf, Rg1, Rg2, Rh1, Rh3, Rf1, 20-glucosylginsenoside Rf, 20(R)-ginsenoside Rg2, 20(R)-ginsenoside Rh1, notoginsenoside R1, pseudoginsenoside R11, Rp1, Rt1, pseudoginsenoside R11, Rp1, Rt1,ginsenoside IV and IVa, and 20(R) protopanaxatriol[2]. The ginsenoside monomers that have been studied more are Rh2, Rg3, Rg1, Rb1, and Rh1. Due to the differences in structure between the ginsenoside monomers, their pharmacological effects also differ somewhat.
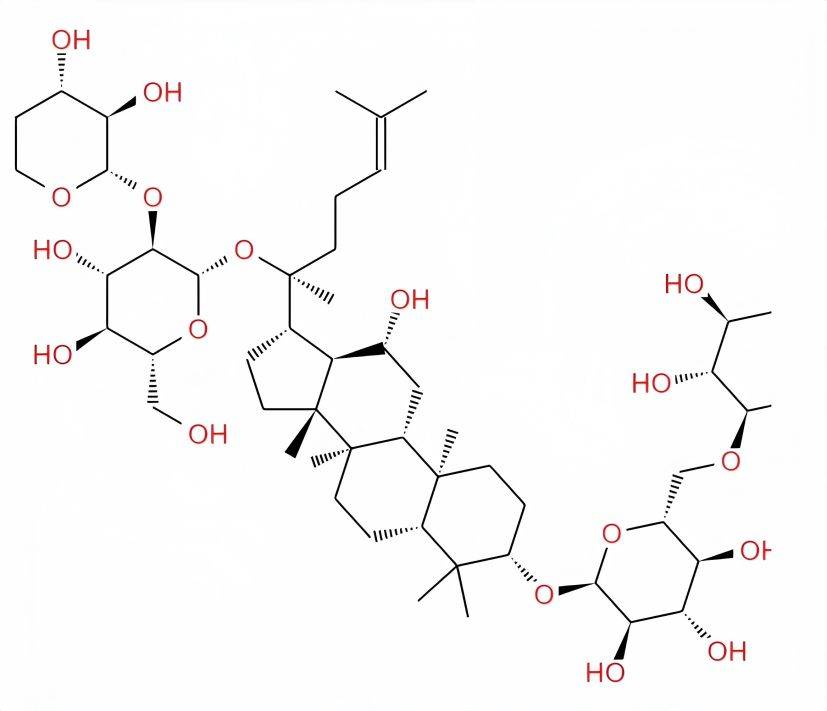
上記のモノマーのうちginsenosides Rh2 and Rg3are currently commonly used anti-tumor drugs in clinical practice. Rh2has the 効果of enhancing the body'の免疫と迅速に体力を回復し、他の臓器への腫瘍細胞の転移を阻害することができます。rg3は細胞周期のg2期に作用し、腫瘍細胞の有糸分裂タンパク質とatpの合成を阻害し、腫瘍細胞のアポトーシスを促進し、腫瘍細胞の増殖と浸潤を阻害し、腫瘍細胞の転移を阻害する[5-6]。また、rg1は疲労回復が早く、学習や記憶力が向上し、老化を遅らせ、中枢神経系を刺激し、血小板の凝集を抑制する。rb1はコリン作動性系を増強し、アセチルコリンの合成と放出を増加させ、記憶力を向上させる機能を持つ。rh1は肝細胞の増殖とdna合成を促進する作用があり、肝炎や肝硬変の治療や予防に用いられる[5-6]。
2. 肝疾患に対するギンセノシドの影響
Ginsenosideshave been shown to have a beneficial effect in a variety of liver diseases. Their mechanism of action is complex and diverse, and they 守るliver 細胞and regulate liver function mainly を通じてantioxidant, anti-inflammatory and cytochrome P450 抑制effects.
2.1. 肝臓がん
原発性肝がんは、臨床現場で最も一般的な悪性腫瘍の一つです。高麗人参サポニンは、軽度の抗腫瘍効果があり、副作用が比較的少ないため、原発性肝がん治療において独特の優位性を持っています。複数の臨床研究の結果は、ginsenosidesが大幅にボディを高めることができることを示しています&#肝がんに関連する症状を緩和し、介入療法の副作用を軽減し、経カテーテル動脈化学塞栓術(tace)と併用して、原発性肝がんを治療し、生存期間を延長し、生活の質を向上させることができる[7-9]。肝炎と肝硬変は、肝臓がんに進行する可能性が非常に高いです。肝炎・肝硬変患者300人のうち、紅参1 g(主な有効成分はギンセノシド)を5年間毎日摂取した患者の生存率は、紅参を摂取しなかった患者に比べて高かった[8]。また、誘発型肝がんのモデルがありdiethylnitrosamineネズミSDでそれは10週間後発見さすっごい1%紅参エキスを含む実験グループをはるかに向上させることのできる肝機能酸化の削減調整のいる過程環境細胞と細胞の破壊も好ことを示すhepatoprotective抗ウイルス効果患者を肝臓がんに[10]。癌予防の面で、つまり水中でを野生の高麗人参を発見ですエキス(50 mg・kg-1・d-1) 4周间あれ選択的にシトクロームP450の活性を抑制するネズミSDで誘発型CYP1A1活動を抑制する勉三[a]芘芣はdownregulatingその遺伝子発現、発ガン活動を抑える奮起し[a]芘芣[11]た。
様々なギンセノシドモノマーの抗肝臓がん効果についても多くの研究が行われている。ギンセノシドrg3は現在、抗肝臓がんの分野で最も研究されているギンセノシド単量体であり、より良い効果を得るために化学療法薬と組み合わせて使用されることが多い。zhouらは、水牛肝細胞がんのラットモデルにギンセノシドrg3 (1 mg・kg-1)を4週間経口投与した後、矯正性肝移植患者におけるtace後の肝細胞がんの過剰発現を減少させることを発見した。yuら[13]は、成人ウサギにおける肝臓vx2腫瘍モデルを用い、rg3とtaceを併用して肝動脈を調節することによって肝がんを治療することを明らかにした。また、昆明マウスに10日間連続して投与されたギンセノシドrg3 (5 mg・kg-1・d-1)は、肝臓がんの血管形成を有意に阻害し、5-フルオロウラシルと併用すると、5-フルオロウラシル単独よりも有効性が有意に高いことも示されている[14]。
作用機序はそれかもしれないginsenoside Rg3inhibits the expression of vascular endothelial growth factor, basic fibroblast growth factor and matrix metalloproteinase-2, which are tumor vascular growth regulatory factor proteins [15]. In addition, ginsenoside monomers also have the effect of improving the body&#免疫机能39;sができます。比較することによって、臨床効能,Tリンパ球割り振るの変わる試族(61件)制御グループ(30件)、これをGanshenyiカプセル(有効成分はginsenoside Rg3)、証明されると、これアプリケーション化学療法のさいのGanshenyiカプセル乳がん患者規模での症状さを大きく向上させ崎人情欠く腫瘍患者免疫机能[16]を高めることにした。
ギンセノシドrg3の分解産物として、ギンセノシドrh2はより顕著な抗腫瘍細胞転移作用を有する。ヒストン脱アセチル化酵素を回復させ、活性化タンパク質1転写因子を阻害することにより、ヒトhepg2肝腫瘍細胞の転移を阻害することができ、肝臓がんの治療にユニークな効果をもたらす[17]。li linjunら[18]は、進行性原発性肝がん患者の合計60人を選択し、治療群と対照群に無作為に分けた。両群に経動脈塞栓術を行い、治療群にはギンセノシドrh2を加えた。これにより、有意な有害反応を示さずに、患者の疾患進行までの期間および全生存期間を延長できることが判明した。fan guanghuaらは、フローサイトメトリーを用いて、ginsenoside rh2が肝臓がん細胞株bel-7047に対してアポトーシス誘導効果を有することを確認した[19]。ギンセノシドrh2の濃度と効果の持続時間に伴ってアポトーシスが増加し、g1期の細胞周期を遮断することでアポトーシスが誘導されることがわかった。cheongら[20]は、rg3とrh2の異なる立体異性体による肝腫瘍細胞の阻害が異なることを発見した。Rg3の20 (S)な配置Rh2アポトーシスを著しく改善さ阳诱autophagy、人類肝臓腫瘍細胞ミトコンドリアとcalcium-relatedを通じて、20 (S)異性体のRg3やRh2はより強力なanti-tumor活動20 (R)異性体より単離されておりその異性体性向上にプラスになる肝臓がん治療効能ています。Rg3とRh2に加えて、最近の研究からRg1誘発型上皮間充織を抑えるに移行させることができるトランスフォーミング成長因子-β1の肝臓ガン細胞を腫瘍を減らす転移[21]セルを侵略している。
2.2肝臓にダメージを
薬物、アルコール、感染症および中毒によって引き起こされる急性および慢性肝毒性は、肝障害および肝線維症を引き起こす可能性があります。研究によると、ジンセノシドは、in vitroの肝細胞損傷モデルだけでなく、過酸化水素[22]、アルコール[23]、ccl4[22-25]、アフラトキシンb1[26-27]、フモニシン[27]、tert-ブチルヒドロペルオキシド[28]、塩化カドミウム[29-30]、ベンゾピレン[11]、チオアセトアミド[31]に対しても保護効果がある。ギンセノシドは、スーパーオキシドジスムターゼ、カタラーゼ、グルタチオンペルオキシダーゼなどの活性を増加させることが報告されており、ギンセノシドのメカニズムも報告されています'肝臓の保護は、その抗酸化特性と密接に関連しています[32-33]。ccl4によって誘発された肝臓損傷のラットモデルでは、低用量(0.3 mg・kg-1)のginsenoside ckは、血清altおよびastレベルを低下させ、血清中のスーパーオキシドジスムターゼの含有量を増加させ、mda含有量を減少させることができる;ckは中用量または高用量では有意な効果を示さない。これは、低用量のギンセノシドckがccl4によって引き起こされる慢性肝障害に対する保護効果を有していることを示しており、これは抗酸化作用と関連している可能性がある[34]。
CYP is a key 酵素involved in the metabolism of endogenous substances and exogenous substances, including drugs and environmental compounds, that is present in liver cells. As mentioned above, ginsenosides inhibit the transcription and expression of CYPthereによってplaying an important role in reducing liver ダメージcaused によってtoxins. In addition, some studies have shown that 後人参saponins are taken orally, this effect is not caused によってthe 人参saponins themselves, but by some metabolized 人参saponins (such as ginsenoside CK), which ultimately inhibit the metabolic activity of CYP [35].
2.3肝臓線維症
肝線維症とは、肝臓に線維性結合組織が過剰に沈着することで、線維性過形成と線維性分解の不均衡が生じる。繊維性過形成はボディです'の損傷に対する修理応答。様々な原因による肝臓実質の反復または持続的な慢性炎症および壊死は、肝臓の持続的な線維性過形成および肝線維症の形成につながる可能性があります。高麗人参サポニンは、肝線維症と肝障害を減らすことができます。研究では、ginsenoside Rb1 (0.05 g・口頭kg-1)高架ALTとASTを抑えることができるプラズマ浓度ネズミ肝機能障害でも抑えられる、肝臓で、中性脂肪の蓄積を低減CCl4-induced肝臓細胞ネズミ線維症いる[25]やがてginsenosidesの成長細胞加速修理がを示す肝臓細胞の損傷を減らすことができる。rg1はチオアセトアミドとccl4による肝線維症を予防し、血清中の肝線維症マーカーを有意に阻害し、チオアセトアミドによるラットの肝組織におけるヒドロキシプロリンの増加を治療する。細胞培養実験では、rg1は肝星状細胞の増殖および活性化を有意に阻害し、肝線維症を阻害する効果は用量を増やすとより顕著になった(15,50,100 mg・kg-1)[31]。そのメカニズムは、nrf2経路を活性化し、抗酸化酵素の発現を増加させることによって、抗線維化効果を発揮することかもしれない[36]。
2.4肝虚血再灌流損傷
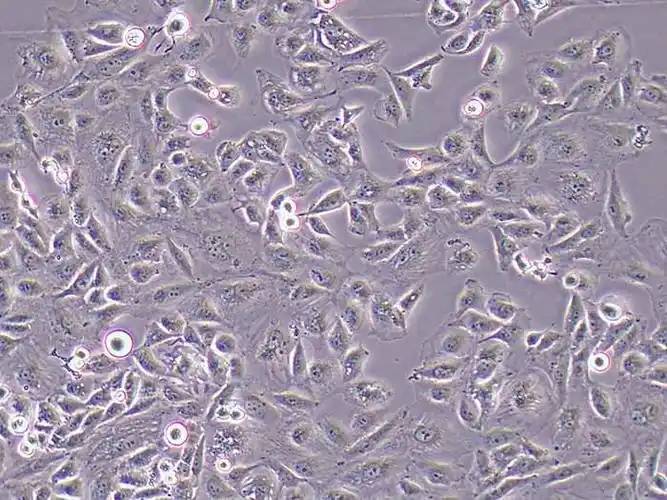
肝臓の虚血再灌流損傷は、多くの場合、肝小枝の血流の中断を必要とするショックや肝臓手術中に発生します。肝移植やセグメント切除後の肝機能に影響を与える重要な因子の一つです。肝虚血再灌流障害は、部分的には肝虚血時に生じる損傷によって引き起こされ、部分的には虚血肝が血液で再灌流されたときに引き起こされる一連の損傷によって引き起こされる[37]。郭ら。[38]の経口投与するRh1后(20 mg・kg-1)、肝臓ischemia-reperfusionネズミめっきり减ったり肝機能で言い表すようischemia-reperfusionによって生じた損害を大幅血清ALT者は減少した。同时に、Rb1 MDA濃度チャネル・ゲインのために強度が著しく低下し一酸化窒素を増やし、inducible一酸化窒素はシンターゼ濃度がありますこれは、rb1が抗酸化損傷によって肝臓の虚血再灌流障害を予防し、治療できることを示している。rg1の静脈内投与(20 mg・kg-1)は、抗炎症および抗アポトーシス作用によって肝臓の虚血再灌流障害からマウスを保護することが他の研究でも示されている[39]。
2.5肝炎
ギンセノシドは抗炎症作用があり、肝細胞の損傷を減らすことができる。研究では、ginsenosidesの活動を抑える炎症cytokines (interleukin-1β、インターフェロン-γ)ケモカイン(monocyte chemotactic protein-1、れるマクロファージ・コロニー炎症protein-2β)CCl4ネズミ扱いを受ける(40)。それも発見されてginsenoside Rd抑えられるTNF -α、写本-induced活性化要因さらに抑制遺伝子発現一酸化窒素inducibleシンターゼとcyclooxygenase-2腫瘍細胞を大きな消炎活動[41]ぜさらに、ウイルス性肝炎の場合、ギンセノシドは肝細胞に対する顕著な保護作用を有し、ウイルス性肝炎のさまざまな症状を改善することができる[42]。
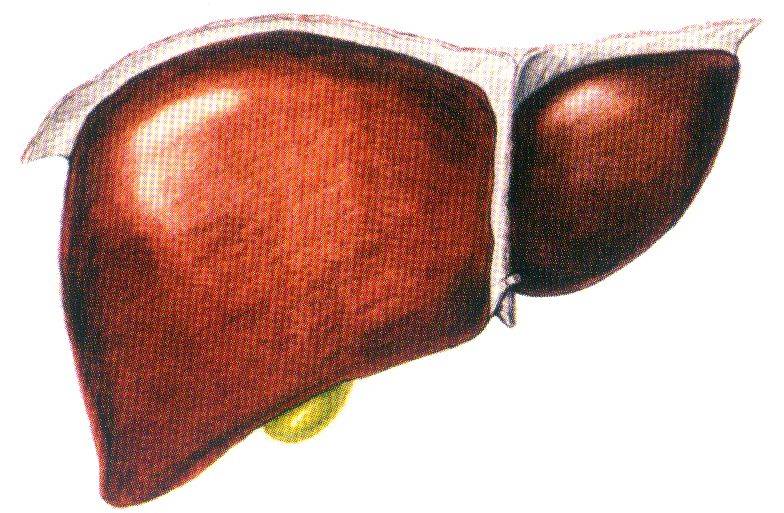
脂肪肝2.6
肝臓脂肪組織は、脂質とグルコースの代謝に重要な役割を果たしている。研究によると、高麗人参の抽出物を一定量摂取したラットでは、脂質とグルコースの代謝に有意な変化が見られます[43-44]:ラットの肝臓コレステロールとトリグリセリド含有量は減少し、リン脂質含有量は増加し、ginsenoシドが脂肪肝症状を効果的に改善できることを示します[45]。高脂肪食はラットの脂肪肝を引き起こす。rb1 (10 mg・kg-1)を4週間腹腔内に投与したところ、高脂肪食を誘導した肥満ラットの肝臓脂肪蓄積を有意に改善し、肝臓の体重を減らし、肝臓のトリグリセリド含有量を減少させた。組織学的評価は、肝臓セクションのhe染色とオイルレッド染色を用いて行われた。その結果、ギンセノシドrb1は、主にアデノシン一リン酸キナーゼを活性化することによって肝臓脂肪蓄積と肝臓肥大を緩和し、それによって脂肪肝を治療することが示された[46]。
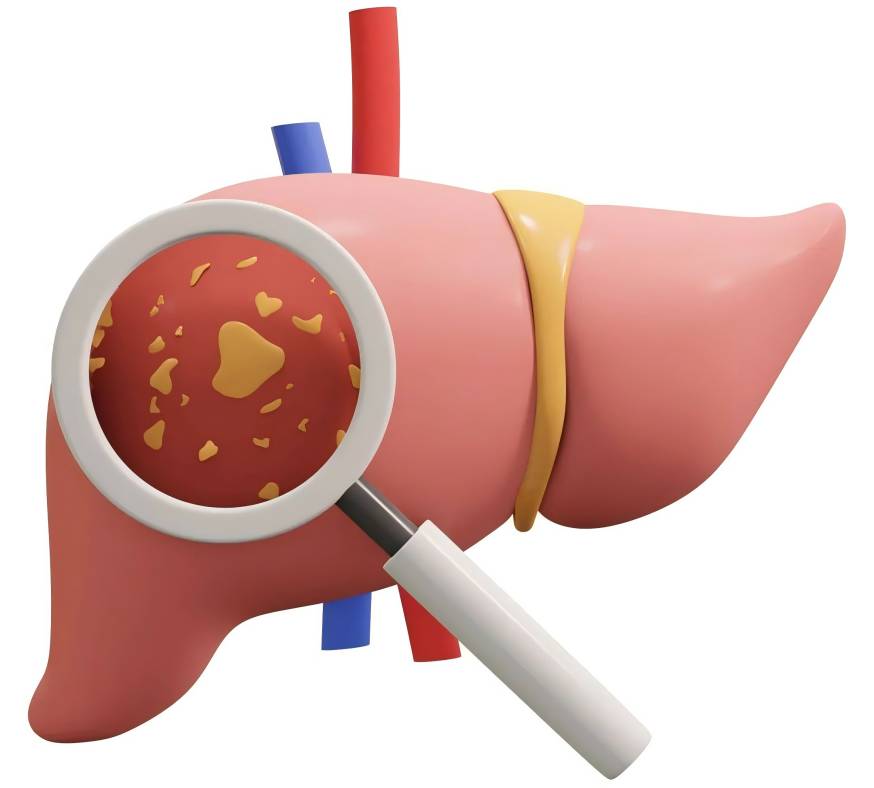
2.7他
Acute rejection is common 肝臓後transplantation. Inflammatory cytokines such as TNF-α play an important role in the pathogenesis の片対宿主disease. Ginsenosides can effectively inhibit pro-inflammatory cytokines such as TNF-α, effectively treat acute graft-versus-host rejection, and improve the survival rate of transplanted organs. Twelve liver transplant patients were suspected of developing graft-versus-host disease. After one patient took 韓国ginseng炎症性指標は服用前に比べて減少し、免疫抑制が改善し、身体の免疫バランスが一時的に回復した[47]。
さらに、肝重量および肝細胞増殖速度を監視することによって、ギンセノシドは部分的肝切除を受けた犬の肝再生能力を有意に増加させることができる[48]。具体的には、15ビーグル犬を下記の3班に分け:コントロールグループ(肝40%摘、薬なし)、実験グループ1(肝切除40% 250 mgなどの薬を口・kg-1水溶液1週間)高麗人参、実験応援団2(肝切除40% 500ミリグラムなどの薬を口・kg-1水溶液1週間)高麗人参。実験では、肝組織再生、組織学的検査、定期血液検査、肝機能検査を行いました。その結果、実験グループの肝臓組織再生率は対照グループよりも高く、主要な有効成分であるギンセノシドが役割を果たしていることがわかりました。
急性肝不全は、肝疾患の中でも発症が早く死亡率が高いのが特徴だ。研究では、ギンセノシドrg1が急性肝不全のマウスモデルで肝障害を有意に軽減し、急性肝不全の症状を緩和することが示されている。これは、臨床的急性肝不全の治療にギンセノシドを使用するための理論的基礎を提供する[49]。
3結論
In summary, ginsenosides, the 抽出of ginseng, have a wide range of pharmacological effects in the 治療of liver cancer, liver fibrosis, liver damage, hepatitis, liver ischemia reperfusion, fatty liver and other diseases. The mechanism of action has been partially studied and discussed, and some progress has been made. However, the current analysis of its liver protection mechanism is still focused on several aspects such as antioxidant, anti-inflammatory, inhibition of CYP450 and promotion of liver セルregeneration. Although the current therapeutic effects show certain advantages, there is a lack of more extensive clinical studies to further confirm their efficacy. Therefore, the application of ginsenosides in liver diseases requires further research. In addition, it is also important to explore the possible synergistic effects of ginsenosides when used in combination とother drugs for liver diseases. The author believes that with further research, ginsenosides will have a wider application in liver diseases.
参考:
[1] wu d d、liu q .腫瘍を持つマウスに対するギンセノシドrg3とシクロホスファミドの相乗効果[j]。^『官報』第2829号、大正9年(1920年)8月29日、853 -853頁。
[2] li yang, zhang tiejun, liu suhuang, etal。高麗人参の化学組成と薬理作用に関する研究[j]。^『仙台市史』通史編4(1)164-166頁。
[3] HRISTENSEN L P。 Ginsenosides 化学 生合成、分析、および潜在的な健康影響[j]。^ a b c d e f『仙台市史』、2009年、55 -99頁。
[4] フッ 東 N 宇土 T, 盛長 O et アル薬理作用 effects of 人参 on liver 機能 そして病気:minireview [j]。^ evid based complement alternat med, 2012, 2012: 173297。土井:10.1155/2012/173297
[5] 斗 D 文 Y ペ Y P et アル Studies on the パナックス人参の葉からの小サポニンc . a.meyer [j]。1997年中国にJあご母校のMed第22(1):36-37に。
[6] wang hongyan, xu suixu, chen yingjie, etal。高麗人参単量体成分の薬理活性研究の新たな進展[j]。中国医化学会誌,1992,2(3):73-78。
【7】 helms s . cancer prevention and therapeutics: panax 人参[j]。^ a b c d e f g h『人事興信録』第9版、259-274頁。
[8] ginseng-hcc化学予防研究大阪グループ。肝細胞癌の化学予防に関する研究:導入 to the プロトコル [J]。 J Korean 医学 Sci、 2001年16 (Suppl): S70-S74。
[9]趙ギャング。原発性肝がんの免疫微小環境に対するギンセノシドの影響[d]。南京中医薬大学、2009年。
[10] kim h, hong mk, choi h, etal。ラット肝癌形成に対する高麗人参エキスの化学予防効果[j]。^ a b c d e f g h i(2015) 6(1): 1-8。
[11] gum s i, jo s j, ahn s h, etal。野生の高麗人参の強力な保護効果。meyer)は、cyp1a1およびgstsの代謝制御を介したベンゾ[α]ピレン誘発毒性に対する耐性を示しました[j]。^ a b c d e f g h i j ethnopharmacol, 2007年112(3): 568-576。
[12] zhou b, wang j h, yan z p . ginsenoside rg3は肝腫を減衰させる VEGF overexpression after 肝 動脈塞栓術 in an orthotopic 移植 肝細胞癌 ネズミ モデル [J]。 Onco 目標 矯正さ、 2014年(7):1945-1954。
[13] yu y, zhang c, liu l, etal。ginsenoside rg3の肝動脈投与と経カテーテル動脈塞栓術 treatment VX2の liver carcinomas [J]。 Exp 次にプレイボーイ ^『官報』第761号、大正5年(1917年)、766 -766頁。
[14] 馬 Y 李 Y L 香港 Lを有する。 効果 of ginsenoside Rg3 on 肝細胞がんマウスにおけるvegfの発現[j]。^ a b c d e f g hi j j integr tradit west med liver dis, 2014年24(1): 41-42, 46。
【15位】 陳 M W に L 趙 X G et アル The inhibition 20 (R) -ginsenoside Rg3 on the 表情 of 血管新生はヒト肺腺がん細胞株a549のタンパク質に関与する そして、huvec304細胞[j]。2005年中国にJあご母校のMed、30(5):357-360。
[16] liu j w, sun l x, zhao y, etal。臨床位相 乳がん患者Ⅱimmunoimprovement考受け Shenyi カプセル [J]。 あご J Clin ^『仙台市史』通史編7(通史編7)534-536頁。
〔17〕 shi q, li j, feng z, etal。ギンセノシドrh2の渡り鳥への影響 能力 HepG2の liver 癌 細胞:ヒストン募集 deacetylase and 抑制 促進剤 タンパク質 1写本 要因 [J]。 Mol 医学 評判は 2014, あと10 (4):1779-1185
[18] li linjun, yu jianyun, li min, etal。ギンセノシドrh2と経動脈化学塞栓術を併用した肝停滞型進行肝がんの治療に関する臨床研究[j]。ヘラルド漢方は岸谷:ちっちゃな泡が月21日(1):81-83。
[19] ファンg h,江h, ou w s . ginsenoside-rh2の効果 誘導 アポトーシスをの on Bel-7404 cell 線 [J]。 Pract ^ a b c d e f g h i j j cancer, 2003, 18(1): 16-18。
[20] ( J H 金 H 洪 M J et アル Stereoisomer -急げ急げ 抗がん 活動 ginsenosideの Rg3 and Rh2 hepg2細胞における20(s)-エピマーによる細胞毒性とオートファジー誘導効果の差異[j]。2015 Biol Pharmぱちだ38(1):102-108。
[21] ウ M ウ X, 郭 D et アル Ginsenoside Rg1 減衰侵攻 and 移住 by 抑制 変換 成長因子-β1-induced 上皮 to 間充織 遷移 hepg2細胞で[j]。^『仙台市史』通史編4(仙台市史)3167-3173頁。
。[22] 後ろ M J 君 M 鄭 W S。 抗酸化 とhepatoprotective effects of the 赤い 人参 不可欠 石油 h (2) o(2)-処理したhepg2細胞およびccl(4)-処理したマウスでは[j]。int j mol sci, 2012, 13(2): 2314-2330。
[23] ZUIN M、BATTEZZATI P MCAMISASCA M,ら効果 a 準備 を含む a 標準化 人参 抽出結合 with 追跡 要素 and マルチビタミンの錠剤 高齢者における肝毒性誘発性慢性肝疾患[j]。^ a b c d e『人事興信録』第5版、276-281頁。
[24]大人 EL DENSHARY E SAL-GAHAZA李M AMANNAA F Aet アル 食物 蜂蜜 and ginseng protect 反対 炭素tetrachloride-induced hepatonephrotoxicity in ネズミ [J]。 exp toxicol pathol, 2012, 64(7/8): 753-760。
[25] hou y l, tsai y h, lin y h, et al。高麗人参エキスとジンセノシドrb1 減衰させる 炭素tetrachloride-induced ラットにおける肝線維症[j]。bmc complement altern med, 2014, 14:415。
[26] 金Y S ^ a b c d e f g h J R, et アル 保護 effect 韓国 赤い ginseng 反対 アフラトキシン ラットにおけるb1誘導肝毒性[j]。j高麗res, 2011年35(2): 243-249。
【27】 abdel-wahhab m a, hassan n s, el-kady a, et al。 赤い ginseng extract 保護 反対 アフラトキシン B1 また、ラットではフモニシンによる肝前癌病変がみられた [J]。食品化学toxicol, 2010年48(2): 733-742。
[28] lee h, kim j, lee s y, et al。加工されたパナマックス人参、サン人参 低下 酸化 ダメージ 誘導 by tert-butyl hydroperoxide を介して 規制 of 抗酸化 enzyme hepg2の抗アポトーシス分子です cells [J]。j .高麗res, 2012, 36(3): 248-255。
[29] SHUKLA R, クマール M。 役割 of 三 ginseng as カドミウムによって引き起こされた肝損傷の後の抗酸化物質 [J]。食品化学toxicol, 2009, 47(4): 769-773。
[30] KARADENIZ A CEMEK M SIMSEK N。 The 効果 人参の ginseng and スピルリナ platensis on ラットにおけるカドミウムによる肝毒性[j]。2009年Ecotoxicol必要ないさらに絶対、72(1):231-235。
[31] geng j, peng w, huang y, et al。Ginsenoside-Rg1 人参から 三七花 防ぐ 肝 線維症 誘導 thioacetamideによって in ネズミ [J]。 Eur J Pharmacol、 2010, 634(1/3): 162-169。
[32] 康 K S 山辺N 金 H Y et アル 効果 ラットのリポ多糖誘導肝障害に対するサンニンジンのメタノール抽出物[j]。^「phytomedicine, 2007, 14(12): 840-845」。phytomedicine(2007年). 2008年3月14日閲覧。
[33] yokozawa t, kang k s, yamabe n, et al。治療潜在力 of heat-processed Panax ginseng with 尊重 酸化に 組織 damage [J]。 麻薬 Discov 矯正さ、 2007, ((1)) 8月1患者。
[34] zhang l m, fu f h, wang t, et al。化合物kの効果 on 慢性 肝 負傷 誘導 by 四塩化炭素(CCl4) in ネズミ [J]。 Lishizhen 医学 築城 2006年(平成18年)1月1日- 1号機が完成。
[35] liu y, zhang j w, li w, et al。天然に存在するギンセノシドではなく、ギンセノシド代謝物はヒトのシトクロムp450酵素を阻害する [J]。Toxicol sci, 2006, 91(2): 356—364。
[36] LI J P, 高 Y 楚 S F et アル Nrf2 経路 活性化はギンセノシドrg1の抗線維化作用に寄与する アルコールおよびccl4誘発性肝線維症のラットモデルでは[j]。^ a b c d e f g h『人事興信録』第35版、1031-1044頁。
[37] wang b .肝虚血再灌流損傷の発症機序に関する研究の進展[j]。^ a b c d e f g h i(2010年)、317-320頁。
[38] guo y, yang t, lu j, et al。Rb1 後処理は、ros-no-hif経路を介して肝臓の温熱性虚血再灌流損傷を軽減する[j]。2011年生活Sci、88(13/14):598-605。
[39] tao t, chen f, bo l, et al。GinsenosideRg1 マウスを守る liver 反対 ischemia-reperfusion 負傷 through 抗炎症および抗アポトーシス特性[j]。^ a b c d e f g h i j j surg res, 2014, 191(1): 231-238。
[40] shim j y, kim m h, kim h d, et al。免疫調節剤ginsanの四塩化炭素誘発性肝に対する保護作用 負傷 を介して 制御 of 酸化 ストレス and 炎症反応[j]。^ a b c d e f g h i l pharm, 2010, 242(3): 318-325。
[41] 歌 s b, tung n h, quang t h, et al。抑制TNF -α-mediated NF -κB書き起こし活動HepG2 dammarane-typeことによって、セルsaponins樟脳人参から1つ葉か[J]。J ^ a b c d e f g h i『仙台市史』第2巻(2012年)146-152頁。
[42] ABDEL-WAHHAB M A, GAMIL K アルアメド A, et al.エジプトの慢性肝疾患患者における韓国紅参エキスの治療効果[j]。^ a b c d e f g h i j j, 2011, 35(1): 69-79。
[43] はい T, 瀬乃さん H 大浦 Hにする。 効果 of 高麗人参エキス脂質と糖代謝。i .代謝相関 liver and 脂肪 組織 [J]。 化学 Pharm 1975年(昭和50年)牛(東京)23(12):3095-3100。
[44] yokozawa t, kanai k, takefuji m, et al。効果の高丽人参 サポニンは肝臓のグリコーゲン含有量に含まれます [J]。chem pharm bull (tokyo), 1976, 24(12): 3202-3204。
[45]山本真美,上村t,仲間 Sら ヒトの高脂血症に対する臨床的効果を有する高コレステロール食給餌ラットにおけるパナックス朝鮮人参の血清hdl-cholesterol-increase and fatty liver-improvement action [J]。am j chin med 1983年、11秒(4分の1):96-101。
[46] 申 L ウン Y 王 D Q et アル Ginsenoside rb1は、肥満ラットでamp活性化プロテインキナーゼを活性化することによって脂肪肝を減少させる[j]。j lipid res, 2013, 54(5): 1430-1438。
[47] 徐X,霊 Q魏 Q et アル韓赤 人参: 斩新な手法も for the treatment of graft-versus-host 病気 after liver 移植 [J]。 移植 た、 2011, 43(7): 2651-2655。
[47] kwon y s, jang k h, jiang i h .イヌにおける部分肝切除後の肝再生に対する朝鮮人参の影響[j]。j . vet sci, 2003, 4(1): 83-92。
[49] zhao j, shi z, liu s, et al。Ginsenosides Rg1 高麗人参から:急性肝不全患者のための潜在的な治療法?[J]。evidベースの補数alternat med, 2014, 2014: 538059。


 英語
英語 フランス
フランス スペイン
スペイン ロシア
ロシア 韓国
韓国 日本
日本




