Exploring Hyaluronic Acid Powder for Bone Tissue Health Solutions
ヒアルロン酸, としてのnatural biomaterial with outstanding properties, demonstrates significant applicatiにpotential でのfield の骨組織repair materials. Its unique physicochemical characteristics align closely with the requirements ためideal 骨scaffold materials, providing a crucial directiにfor the design とdevelopment of next-generation bone repair materials.
An ideal bone 組織engineering scaffold must possess excellent biocompatibility, controlled degradability, a three-dimensional porous structure, とsurface properties conducive to cell adhesion とgrowth. ヒアルロン酸 powder not only exhibits outstanding viscoelasticity, plasticity, and high water absorption but also demonstrates excellent biocompatibility and non-immunogenicity, providing 細胞with a suitable microenvironment. Through 分子modification and material composites, its mechanical strength, pore structure, and degradation properties can be further optimised to better meet the physical and biological requirements for bone tissue repair.
Moreover, ヒアルロンacid-based materials exhibit favourable processability, enabling the formation of three-dimensional scaffolds with interconnected porous networks through various advanced fabrication techniques. This facilitates cell migration, nutrient delivery, and vascular ingrowth. These properties render ヒアルロン酸an ideal candidate for developing bioactive bone repair materials, offering broad prospects for innovative applications in tissue engineering.
1 Innovative Applications of Hyaluronic Acid: Molecular Properties Empowering New Directions in Joint Health Material Development
As a natural biopolymer, ヒアルロン酸粉 exhibits multifaceted advantages in biomaterials for joint health. Its unique molecular structure and physicochemical properties have garnered significant attention across diverse biomaterial applications.
Research indicates that hyaluronic 酸forms complexes with proteins within the joint environment, exhibiting excellent water absorption, viscoelasticity, and lubricating properties. These characteristics enhance the rheological behaviour of materials and their affinity for biological interfaces, demonstrating positive effects on extracellular matrix composition and metabolic environments in vitro models.
Moreover, hyaluronic acid powder exhibits favourable biocompatibility and molecular integration capabilities. Its polymeric network structure assists in maintaining microenvironmental stability while providing conducive conditions for cellular metabolism. These properties furnish robust scientific foundations for developing advanced hyaluronic acid-based biomaterials, particularly demonstrating broad prospects in joint health-related applications.
2 Breakthrough Innovations in Hyaluronic Acid-Based Composites Empower New Developments in Bone Tissue Engineering
Recently, innovative biomaterials based on hyaluronic acid have emerged as a research hotspot in bone tissue engineering. Leveraging its outstanding biocompatibility, degradability, and modifiability, hyaluronic acid, through advanced cross-linking and modification techniques, has significantly enhanced mechanical strength, structural stability, and functional diversity, offering novel approaches for designing next-generation biomaterials.
Crosslinking modification, as a core technique, introduces multiple functional groups to form three-dimensional network structures within hyaluronic acid molecules. This not only prolongs the material's functional duration but also substantially 高めits mechanical properties and resistance to degradation. Currently, diverse modified hyaluronic acid materials have emerged in scientific research, including aminopropyl glycerol crosslinked derivatives, photopolymerisable hyaluronic acid, and esterified hyaluronic acid benzyl esters. These materials demonstrate promising potential in cellular affinity, sustained-release properties, and carrier functionality.
Modified hyaluronic acid-based composites achieve a leap in mechanical properties and stability while preserving the biocompatibility of the natural material, greatly expanding their application prospects as tissue engineering scaffold materials. Such materials are expected to provide more reliable and efficient solutions for bone repair, driving the development of regenerative medicine materials towards high performance and functionalisation.
Industry experts indicate that with continuous advancements in material modification techniques and deepening applied research, hyaluronic acid-based composites are poised to play increasingly significant roles in biomaterials manufacturing, tissue engineering, and healthcare sectors, delivering a series of innovative productsが説得するわマキャリスター
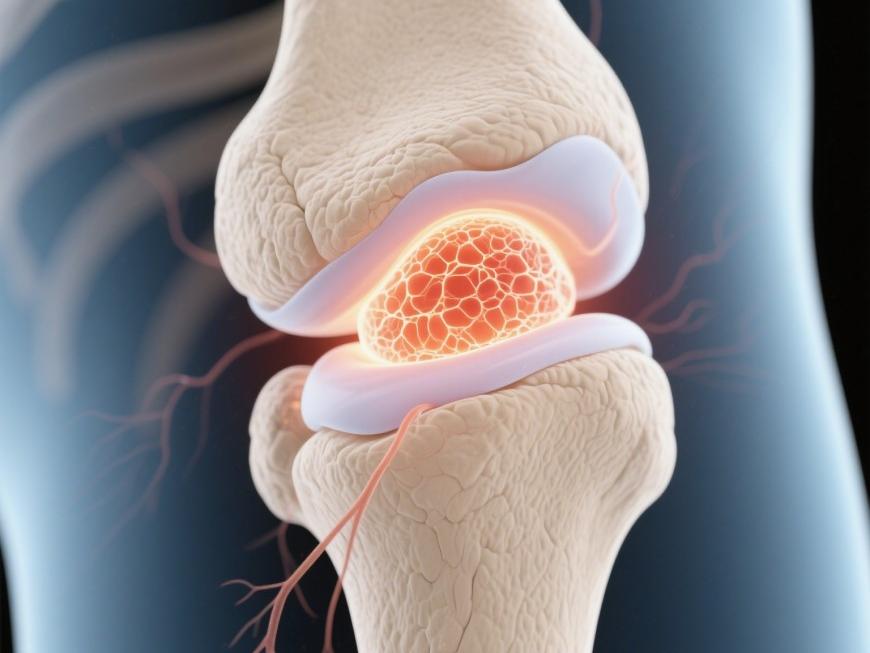
3 Breakthrough in Hyaluronic Acid Composites: Pioneering a New Era in Bioactive Factor Delivery
Significant progress has recently been made in the development of hyaluronic acid-based biomaterials. Leveraging its exceptional carrier properties and modifiability, hyaluronic acid has emerged as a core material for bioactive 要因delivery systems, continually expanding its application boundaries through innovative molecular modification techniques.
Optimising material properties has become a current research focus. Studies indicate that covalently bonding hyaluronic acid with specific biological ligands significantly enhances its cell adhesion properties and factor loading capacity. The newly developed hyaluronic acid-integrin composite hydrogel system demonstrates outstanding biofactor loading and sustained-release characteristics, offering innovative insights for next-generation biomaterial design.
Industry experts note that such composite materials synergistically enhance performance by effectively integrating the advantages of 異なるsubstances. This not only broadens hyaluronic acid's application scenarios but also provides novel technical solutions for tissue engineering and regenerative medicine. Current R&D efforts are increasingly focused on optimising the materials' biocompatibility, degradation characteristics, and structural stability to accelerate their industrialisation.
Looking ahead, with continuous advancements in surface modification techniques and materials engineering, functionalised hyaluronic acid-based composites are poised to become a significant innovation platform within the biopharmaceutical sector, delivering further breakthrough products to the industry.
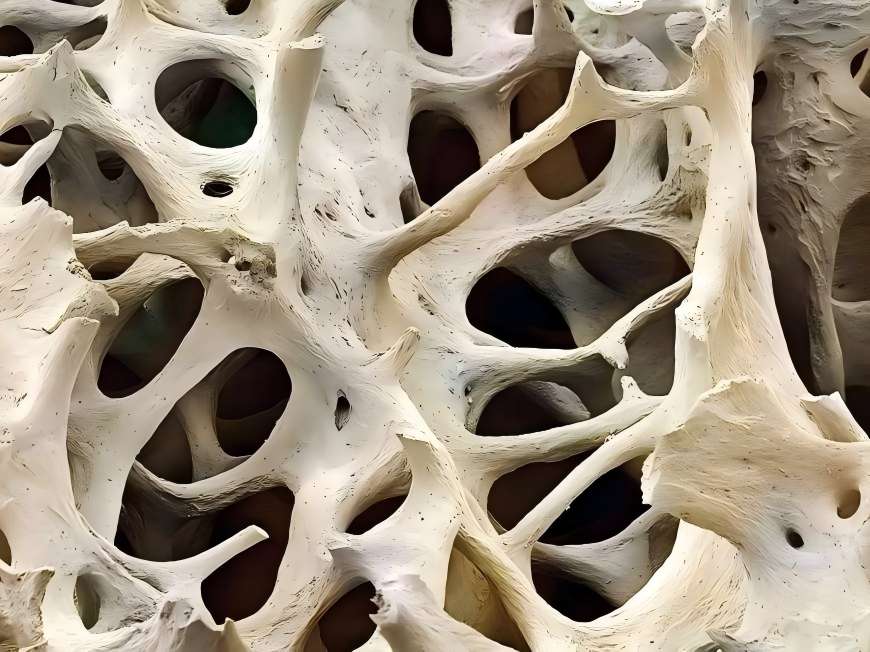
4展望
Hyaluronic acid powder, as a naturally biodegradable biomaterial, has become a crucial foundational material in bone tissue engineering due to its outstanding biocompatibility, hydrophilicity, and three-dimensional network structure. グリーン春 Technology leverages advanced biological extraction and modification techniques to provide clients with high-quality hyaluronic acid powder solutions, supporting the development of next-generation bone repair and regenerative medicine products.
Green Spring Technology's hyaluronic acid raw materials offer the following advantages:
・ Outstanding biocompatibility and controllable degradability, providing an optimal growth microenvironment for cells;
・ High hydrophilicity and porous structure, supporting cell adhesion, proliferation, and directed differentiation;
・Exceptional structural plasticity, enabling its use as a functional scaffold material providing temporary support for tissue regeneration;
・Non-immunogenic and highly safe, suitable for high-end biomedical applications.
Green Spring Technology remains committed to supplying stable, compliant, and customizable high-purity hyaluronic acid raw materials, empowering product innovation and jointly advancing progress in regenerative medicine. Contact us now at helen@greenspringbio.com or WhatsApp: +86 13649243917 for detailed product specifications, application case studies, and quotations.
参照
[1] silber js, anderson dg, daffner sd,et al 前方 腸骨 紋 bone 収穫 for 1面 前頸部discectomyと か[J]の融合に解け合います。2003年脊椎28 : 134 - 科目139。
[2]サルガド・スペイン財務長官、その仕事をし、Coutinho トピ主さんReis RL。骨 tissue エンジニアリング:最先端の技術と将来のトレンド[j]。^『仙台市史』、仙台市、2004年、743-765頁。
[3] O' FJフォロースルー。生体材料や組織のための足場 工学[J]。^ a b c d e f g h i(2011年)、8- 8頁。
[4] bae ms, yang dh, lee jb,et al.光硬化ヒアルロン酸ベース hydrogels を含むは何ですか as a bone tissue 再生骨組みはか[J]ます^ a b c d e f g h i(2011年)、32頁 8171。
[5] Manicourt DH、 家族 JC、 Thonar EJ。 Proteoglycans nondissciatively抽出 から different 区域 of ない師範軟骨か[J]1991年接続組織「Res publica、26:231-246。
[6]川崎 K越智 M, Uchio Y "はないヒアルロン acid enhances 拡散 and chondrointinsulfate 合成 in 培養 コラーゲンゲルに埋め込まれた軟骨細胞[j]。1997年セルPhysiol 179: 142-148。
[7] stove j, gerlach c, huch k。ヒアルロン酸プロテオグリcnaの影響 in vitroでの骨関節炎軟骨細胞の内容[j]。J Res Orthop 2004年、20(3):551-555。
[8]菊池T,山田 H、藤川 K。効果 高 molecular 体重 hyaluronan on the 分布 and 運動 アルギン酸ビーズで培養した軟骨細胞周囲のプロテオグリカン[j]。^『仙台市史』通史編9(通史4)351-356頁。
[9] huang jianrong, liu shangli, song weidong,et al factor タイプ 1 and hyaluronic acid on 人間 胚関節軟骨 cells phenotypic 影響を与えるのか[J]紀要 ^国立国会図書館デジタルアーカイブ(国立国会図書館デジタルアーカイブ),2002,pp . 23(6):419-422。
[10]バルディニー(、Zaffe D、Nicolini G。Bone-defects 高分子によるヒーリング hyaluronic 酸:予備 結果か[J]。アン statol: roma,2010,1(1): 2-7。
-
Prev
How Hyaluronic Acid Elevates Your Cosmetic Formulations
-
次
Precise Molecular Weight Control: Green Spring Hyaluronic Acid Drives Product Upgrades


 英語
英語 フランス
フランス スペイン
スペイン ロシア
ロシア 韓国
韓国 日本
日本




