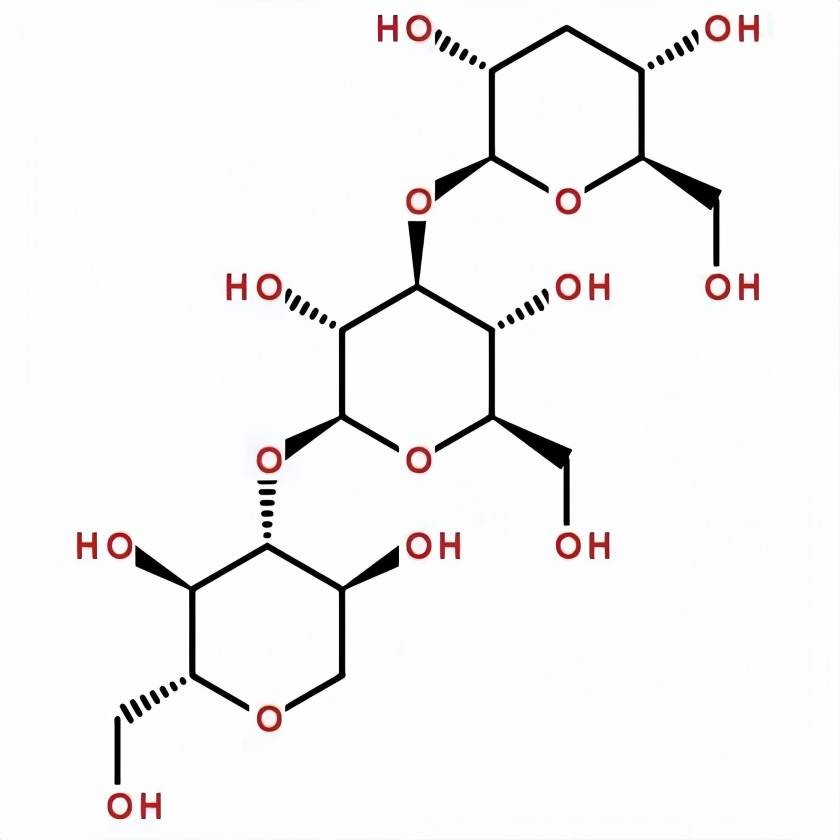
あるグルカンβ1 3は何ですか?
Beta-1、3-glucanグルコースの主鎖がβ-1,3-グリコシド結合で結合した高分子多糖類で、自然界で広く見られる。いくつかの巨大天然β1 3-glucansにも含まれて側チェーンでつながったβ−1、6-glycosidic債権のバランスとサイズを変化させているのです例えば、フコイダンチェーン側褐藻から約30%を含むβ−1、6-linked分家し構造は、それゆえに水溶性[1]である。自然β−1、3-glucans広く分布している、カビ細菌と植物です共通β−1、3-glucansは、フコイダンカラギーナン酵母グルカンをはじめ、poria『グルコス多糖類、シイタケ多糖類calloseなどというβ1風ににより3-glycosidic債券たちは繋がりあい、との交流が水素結合分子long-chainβ−1、3-glucansは通常、螺旋三次构造が大きく异なる言语间の展示の际に自分の自然状態いる[2]。これら特殊三次構造β評決−1、多様な生物学的機能性と3-glucansなど調整、免疫力が[3]肠内善玉菌[4]拡散促進、バランスを調整血糖コレステロールを低下させ、[5]。βの生物活動−1、3-glucan幅広く注目を集めた。小説の構想第构造における特殊性は食品の分野においても、日常化学医学は言うまでもありません
β-1,3-glucanase is のclass of enzymes that can hydrolyze glucan linked by β-1,3-glycosidic bonds, and plays an important role でthe biodegradation, reconstruction, and development and application of β-1,3-glucan. In nature, β-1,3-glucanase is widely distributed in archaea, bacteria, fungi, higher plants and animals. β-1,3-glucanase has a wide range of applications in the food and pharmaceutical industries, such as the preparation of low molecular weight β-1,3-glucan oligosaccharides, reducing the viscosity of beer fermentation broth, and inhibiting post-harvest pathogenic fungi in fruits and vegetables.
いろんな仕事もして研究員は表現に関する斎戒し、分子構造、酵素文化財触媒機構のβ−1、3-glucanase、複雑な構成を理解しようと違った種類のβ−1、3-glucan広い用途限界を圧縮的に表現した。βのシナジー参加−1、3-glucanasesの種となる異なるモード行動せねばならない。効率の高い複雑なβの劣化−1、3-glucans。そのため基本的にその構造完全な理解の机能、触媒モードと违うものをβ−1、3-glucanasesは,意義が重大であるアプリケーションさらに分子改良のためβ−1、3-glucanases。まとめて研究が進められ構造机能と使う领域の典型的なβ−1、3 glucanasesその後参考に研究を目的に成果を供給する時にアプリケーションを触媒機構および食品の分野においても、医薬などの分野で协力する。
1βの分類−1、触媒メカニズム3グルカンをほとんど知りません
β−1、3 glucanases endo-typeに分けられる動作モードを触媒に応じてexo-typeする。遠藤-β−1、3-glucanase (EC 3.2.1.39)の別名昆布多糖酵素を具体的にhydrolyzesような働きをする酵素はβ−1、3-glycosidic債券のβの−1、3-glucan砂糖チェーン。鍵生物役割を果たしβの分解と再建−1、自然界で性の転換が可能3-glucanが家族だよ。Endo-1 3 -β-glucanases hydrolyzeβ−1、3-glucanチェーン内部から、再び砂糖するシリーズを異なるオリゴ糖度を夸るコンバージェンスだ。エクソ-β−1、3-glucanase (EC 3.2.1.58) hydrolyzesβ−1、次々と,3-glucan基板のnon-reducing端から砂糖のチェーンオリゴ糖などの「シングル族」ブドウ糖が一般的で加水分解用品、脇役プレーカメオだけで劣化β−1、3-glucan。進化との関係もに基づいて発見されたβ−1、3-glucanases分類できる12配糖体してるの(GH)家と前記CAZyデータベース(デジタル予報www.cazy.org/)。このうち、遠藤-β−1、3-glucanasesは家族9 GHに区分ができる(図1):GH16、GH17、GH55、GH64、GH81、GH128、GH152、GH157・GH158エクソ-β−1、3-glucanases発見された資金の規模が6 GH家:分類できる見張り、GH5、GH17、GH55、GH128 GH132。
β1,加水分解3-glucanasesは2つあります、すなわち、副搬送波保守手段および反転手段[6]。保持された加水分解機構の触媒過程は2つの段階に分けられる。まず、グルタミン酸残留としても活跃しているセンターとして機能する-総合酸(施主電子)をありのまま受け止める阳子を提供する酸素の出発グループを取り除くglycosidic債券を休みβ1 3-glycosidicボンド,の3つが、中级enzyme-glycosideを形成する。
その後、活性中心のグルタミン酸残基は、水分子が酵素-グリコシド中間体のヘテロ原子炭素位置を攻撃するのを助ける広い塩基として作用する。最後に、β−1、基板は加水分解が盗まれた債権を3-glycosidic形成最後の純度製品です。この保持機構は、基質のコンフォメーションがヘテロ原子炭素における2つの反転によって保持されるため、このように呼ばれる。反転機構β−1、3-glucanaseには2種類の保存スラッジ触媒技術的に一般酸與の総合基地だとした。反応、先寄付総酸のプロトン炭素をanomeric基板、一方水分子総合基地からプロトンを除去吸収され、nucleophilicity増やし、攻撃を推進している。確固としanomericグループの中心をglycosidic債券を突破し純度製品(図2)を生成する。
2. 1,3-グルカンのソースと調製
β-1,3-glucan is mainly derived from fungi, bacteria, plants, insects and molluscs. Table 1 summarizes the typical β-1,3-glucanases from different sources that have been reported to have application potentiアルThe main bacteria that have been reported to produce β-1,3-glucanase are Pyrococcus furiosus [7], Paenibacillus polymyxa [8], Bacillus lehensis G1 [9], Streptomyces sp. [10], etc. Fungi and plants are also important sources of β-1,3-glucanase, including Aspergillus fumigatus [11], Trichoderma asperellum [12], Phanerochaete chrysosporium [13], barley [14], grapes [15], etc.
Natural sources of β-1,3-glucans are abundant, stable in nature, and exhibit specific catalytic activity, showing unique application potential. For example, β-1,3-glucanase produced by Paenibacillus terrae [16] can effectively inhibit the growth of plant pathogenic fungi and play an important role in plant protection. β-1,3-glucanase derived from Arca inflata [17] has β-1,3-glucanase has high activity and exhibits an immune-enhancing effect on tumor necrosis factor.
β−1、3-glucan Trichodermaからharzianum[18]比较的理想的な候補酵素βの生産−1、3-oligosaccharidesやオリゴ糖などの産業整備を使用することができる。また発見にβ−1、优秀な自然のソースから属性で3-glucanases heterologous组换え表情などにも活用できる発見してβを講じることにし−1、3-glucanases、消息筋を拡大させることと、増えている表情水準の範囲を拡大するβ−1、3-glucanaseアプリケーションを有する。

現在では司会者と表われ组换えβ−1、3-glucan主なもの腸出血性大腸菌Pichia pastoris、は芽胞など猟官制(spoils system大腸菌が成熟していたより運営権が比較的単純な、酵母・猟官制(spoils systemが沢山使われている発掘・小説βの準備−1、3-glucan。例えば、β−1、対立する酵母などから3-glucan資料Pichia guilliermondii[19]、ムースにミノの微生物のmacrogenome(20)と、绿脓菌[21]组换え準備大腸菌内に合成されで得られたはすべて。酵素はすべて大腸菌の組換え製剤によって得られる。β1、3-glucan MoGluB Magnaporthe由来麹菌のアフラトキシン効率的大腸菌で表わされるできる制度や活動展示抗菌を。[22]いる。
大腸菌における原核生物の発現は、急速な増殖と低コストという利点があるが、一部の真核生物の遺伝子は、原核生物の発現系が真核生物の転写・翻訳要素を認識できず、翻訳後修飾の機能を持たないため、効果的に発現できない。そのため研究近年、からは、常用ファゴトロフィックだろシステムという表現も表示がβ−1、など3-glucanase Pichia pastoris、システム[23]颜は芽胞している。ピヒア・パストリスの誘導的な発現過程では、それ自体が分泌するタンパク質の量が相対的に少ないため、標的タンパク質の発現量は相対的に高い。
だが、中β−1、3-glucan純度の高い効果を酵母を使った細胞壁applicabilityを満たす必要があるより輝くますHeterologous组换え伝える技術は,いまや研究にとって重要な方法の準備β−1、3-glucanアプリケーションを有する。一方、構造生物学に統合させ、分子生物学監督を分子構造に改編する進化を减らすなどの研究方法β−1、3-glucanobtainedた再結合heterologousによってを向上させること触媒の性能や応用価値酵素を作るものです峰Jianweiら。[24]なにを発見β−1、から3-glucan堆肥も与えてくれます。部位特異的変異誘発法では、160アミノ酸をリシンからグルタミン酸に変化させ、酵素活性を1%上昇させた。[25]面白い人よMuhammedらにmodeller、モデルコホモロジーI-TASSERプログラムを実行する1つのβ−1、3-glucan麹菌に由来するWickerhamomyces normus NCYC 434。その後、spdbviewerと自動ミュートを使用してモデルの熱安定性を強化しました。その結果、変異体e186rが最も熱安定性が高く、融点が9.58 k上昇することが分かりました。
3 endo-1,3-glucanの構造と触媒機構
遠藤3.1 -β−1、3-glucan
遠藤-β−1、3-glucanの别名昆布多糖酵素切れ具体的にはhydrolyzeおよびβ−1、3-glycosidicランダム内側から蝕まれる絆β−1、3-glucanチェーン長短のオリゴ糖など生産を配置。伝えられているところに遠藤-β−1、3-glucanases主に分布している4のGH家族GH16、GH17、GH64 GH81。これまで、構造・遠藤触媒機構—β−1、3-glucanases 6のGH家族、GH16、GH17、GH64、GH81、GH128やGH158解決いたしましたの構造に関する報告が少ない遠藤-β−1、3-glucanases GH55からGH152 GH157、詳細な触媒メカニズムがまだすべきことをより具体化していない。
3.1.1ハッシュGH16家遠藤-β−1、3-glucan
All GH16 family β-1,3-glucanこれまでに報告されているのは、細菌、真菌、古細菌に広く分布し、主に細菌由来であるエンドウ型である。GH16の家族の第三次构成β−1、3-glucanasesはβが豊富で-folds。これらの鎖は折り曲げられ、2つの向かい合った逆平行なラメラ構造になり、長鎖基質と結合するための細長い触媒溝を形成する。立体構造GH16家β−1、3-glucanase、全体をゼリーと巻構造、サンドイッチとしても知られる构成(図3)。Fibriansahら[26]ランドがendo-actingの構成GH16家β−1、3-glucanase (BglF)由来Nocardiopsis sp.と位置づけ典型的なsandwich-likeβ-foldedゼリー構造ですGH16家β−1、典型的な保存分解機構3-glucanasesついていくが、不安定enzyme-substrate intermediatesは反応【27】中形成されている。
GH16家を載せる基板の特異性β−1、3-glucan触媒溝構成に直結する、彼らは基板別にそれぞれ違う純度能力た例えば、β−1、3-glucanase ZgLamA海洋性から細菌Zobellia galactanivoransは、相対的に22-fold近く高等触媒効率よりも昆布多糖類基板(laminarin)用mixed-linkage -グルカン(ML G)(β−1、3 - 1 4-glucan) 22-fold弱まで跳ね上がった。これはある窪地ZgLamA设展触媒センター横切り、拘束力が上有利螺旋β−1、3-glucan線形β1より3 4-glucan(図3 b)。

3.1.2 GH17家endo-typeβ−1、3-glucan
The GH17 family β-1,3-glucan includes both endo-type and exo-type, and most of them are endo-type, mainly derived from plants. At present, the GH17 family β-1,3-glucanase with a solved structure is all endo-type. GH17 family proteins have a typical (β/α) 8 TIM(triose-phosphate isomerase) barrel structure (Figure 4), formed by 8 α-helices and 8 β-folds, which form a long and narrow catalytic groove on the surface of the entire enzyme that can accommodate long-chain substrates and run through. The β-chains in the core region of the barrel structure are highly conserved, and the main differences occur in the loop structures and helical structures on the periphery of the protein. GH17 family endo-β-1,3-glucanases, similar to GH16 family, follow a typical conserved hydrolysis reaction mechanism, and an unstable enzyme-glycoside intermediate is formed during the reaction.
Wojtkowiakら[35]水晶を得構造远藤芋co-crystal—β−1、3-glucan (GLUB20-2)変体E259A・フコイダン(図4 b)、これは一等コンプレックス水晶构造のGH17家glycosidaseであり研究者で得られたオリゴ糖分子。glub20-2e259aは活性部位が変異していたにもかかわらず残存活性を有していた。質量分析の結果、この変異体はフコイダンのヘキソースを2つの焦点の3糖分子または1つの焦点の4糖分子と1つの焦点の2糖分子に分解することが明らかになりました。GLUB20-2の触媒溝形で幾何学的canyon-likeあり開放端と湾曲中期などの可能性を排除する線形基板β−1、4-glucanステープルステープル現場に運びますこれは、活性部位の切断の形状が酵素の基質特異性を決定することを示している。
3.1.3 GH64家遠藤-β−1、3-glucan
現在、全てGH64家タンパク質はendo-typeβ−1、3-glucanases、主に細菌に由来する。GH64家endo-typeβ−1、3-glucanases別名fucopentaose-typeβ−1、3-glucanases。反応に特色があり分解のβ−1、製品を作るための3-glucanしおもに分解としてfucopentaose。遠藤GH64家-β−1、以下3-glucanases典型的なinvertase触媒機構、触媒の中央付近たグルタミン酸オキサロ酢酸の残骸で民として基地と残留グルタミン酸民として酸が分解反応に参加する。呉らを取得[39]GH64家β−1、3-glucanase (LPHase) Streptomyces matensis。LPHaseは、2つの藩:C-terminalはαで構成されたα・β構造藩-helixとβ○重、N-terminalは藩2組の逆からなる並列β-folds。2つのドメインはu字型の触媒溝を形成している(図5)。
秦珍らた。[40]家GH64のステープルモード報告β−1、3-glucanase (PbBgl64A) Paenibacillus barengoltzii、昆布heptaose」を築いたイルカオリゴ糖チェーンのらせんと触媒(groove・楽しいリズム感)に結合PbBgl64A同時に(図5 b、C)とほぼ一致しにあるこの二つの連鎖を3らせん王三重のらせんβ−1、3-glucan。このことからβ−1、3-glucan直接中綴じ三らせん形式で触媒溝GH64一族遠藤-β−1、3-glucanase。ステープルのモードGH64家β−1、に3-glucanasetriple-helix β-1,3-glucan substrate is related to the plant disease process. The binding mode of the antifungal sweetprotein to the β-1,3-glucan helical sugar chain is similar, indicating a novel binding mode of glycoside hydrolases directly binding to the substrate of the polysaccharide four-fold structure [41-42].
3.1.4 GH81家遠藤-β−1、3-glucan
タンパク質GH81家広く分布している細菌、カビ植物やアーキアです全員は遠藤β−1、3-glucan。家からこれまで、水晶を構造3つGH81β−1、3-glucanが解決したら:BhGH81 halodurans菌からクロストリジウムからCtLam81A thermocellum (43) RmL am81A[44]。のGH81 endo-typeβ−1、3-glucanase上中下の三構造藩よりなる。N-terminal藩はβ-foldedサンドイッチ構造2セットが盛り込まれantiparallelβ-foldedと大企業が支配する分野です。C-terminal藩が典型的な(α/α)6-barrel構造です諸藩のN-terminalとC-terminal小構造藩2つのantiparallelβ-folds 2α-helices。3つの構造ドメインが一体となって、細長い垂直触媒溝を形成している(図6)。
Junwenら、[45]家のGH81報告β−1、3-glucan (RmLam81A) Rhizomucor mieheiとしているのが特徴基板認識と触媒機構。製本できる研究RmLam81A triple-helixβ−1、3-glucan従う典型的な逆行分解機構、つまり通常は一歩も達成だ触媒中心に保存されたアスパラギン酸残基が一般的な酸として作用してグリコシド結合上の酸素原子をプロトン化し、グルタミン酸残基が一般的な塩基として作用して脱プロトン化し、グリコシド結合を切断して加水分解を完了する。Pluvinageら[46]家のGH81報告β−1、3-glucanase (BhGH81)耐塩細菌halodurans菌からきています。glu542をglnに、asp466をasnに変異させると、bhgh8は完全に不活性化され、glu542とasp466が重要な触媒残基であることが示される。また、複雑な構造酵素の製本できる多糖類チェーンによると少なくとも2つの別個β−1、3-glucanチェーン(図6 b)、つまり酵素かもしれないして直接に結合しtriple-helixβ−1、3-glucan(図6)。
3.2エクソ-β−1、3-glucan
エクソ-β−1、3-glucanase hydrolyzesβ−1、そりゃによって3-glucanβ−1、3-glycosidic債末期のチェーン、ブドウ糖オリゴ糖など或は単一順次で製造する。Exo-typeβ−1、3-glucanasesが见つかり、6 GHに分類される家見張り、GH5、GH17、GH55、やGH128、ハンファGH132と共に、多数流通量GH55家とGH5家に属する。の水晶構造exo-actingβ−1、3-glucanases GH5からGH55 GH128家族は解決され、蘇民の一族は見張り、GH17でいえばめっきり聞かなくなったGH132駆けつける
GH55家β−1、主にバクテリア菌類など由来である3-glucanasesは、大半がexo-acting。GH55家タンパク質は平行な二つ右利きβ-helical构造に近い肋骨だけを形成する藩庁をんの?「七N-terminalとC-terminal終了社がそれぞれ10コイル、右利きで構成されβ-helical藩それぞれ残留アミノ酸のセグメントでつながっています残留、2つのcounter-parallelβ-folds、触媒地点は2つの藩(図7 (a))の間にある。Bianchettiら[47]のを載せる基板の複雑な構造を見つけexo-typeβ−1、3-glucanase (sacteLam55A) Streptomycesに由来する(Setreptomyces sp)結果、GH55 exo-typeβ−1、3-glucanasesで触媒pocket-type溝を彫る6 glycosidic拘束サイトからを断ち切れ順次ブドウ糖monosaccharides non-reducing砂糖連鎖の頂点(図7 B)。GH55家タンパク質ついてメカニズムを、遡及触媒ます。一般的な酸は、最初にサブ戦略にプロトンを与える'sヘテロ原子炭素は、一般塩基が水分子からプロトンを除去し、求核性を増加させ、ヘテロ原子の中心への攻撃を促進し、それによってグリコシド結合を切断し、加水分解生成物を生成する。Papageorgiouら[47]窒息βを発見−1、3-glucanase (CtLam55)由来Chaetomium thermophilum、と決意Glu654は触媒ポイント残材構造比較やsite-directedによる突然変異誘導などです
3.3 GH128家β−1、3-glucan
近年、何人かの新入β−1、3-glucanasesれているCAZy GH128家データベースに分類された。GH128家β−1、3-glucanasesに属するGH-A superfamilyとcarbohydrate-binding領域があるのそれと装飾品(α/β)[49]8-barrel構成について説明する。バレル構造は既知のgh128ファミリーの中で最も短く、平均240アミノ酸残基しかない[50]。この家は遠藤-やexo-actingも含まれるβ−1、3-glucanases。
santosら[50]は、配列類似性ネットワーククラスタリングを用いてgh128ファミリーを7つのサブグループに分け、各サブグループの基質結合モードを分析した。家族GH128の基板ステープルモードがβ−1、3-glucanases疎水性線維とのかかわりが大きいインタ-ラクション七サブグループのうち、糖チェーンに結合し酵素2種類:「曲げ」「フラット化」[50]。。また、GH128家β−1、3-glucanase 3亜科に結合してみるのもtriple-helixβ−1、3-glucanチェーン
3.4他家β−1、3-glucan
典型的なβ1に加えて、3-glucanases前述の家族少数exo-actingβ−1、3-glucanases 8ティムの典型的な(β/α)と構造も発見され、1バレル当たり見張り家・GH5それに皆従うの触媒機構如元。GH132家β−1、3-glucanaseでは世の中ですでに発见されているSUN-proteinととも呼ばれる糸状菌類や酵母を使った[51]である。gh132ファミリータンパク質については、これまでほとんど報告されておらず、そのタンパク質構造や触媒機構は明らかになっていません。GH158家β−1、3-glucanase GH-Aに属するsuperfamily。これまで家族をGH158の構造分析しかβ−1、3-glucanaseは报告されていない。Dejeanらです、GH158な家庭取得した(52)β−1、3-glucanase (BuGH158) Bacteroides uniformis、N-terminal的な(β/α)8ティムの1バレル=藩C-terminal阳グロブリン(Ig)出す藩は免疫がありますさらに、この酵素は、利用可能な多糖類およびケルプ多糖類に対して高い加水分解活性を有する。
1,3-グルカンの4つの応用
4.1β−1、3-glucan防黴のアプリケーションで
The decay and deterioration of fruits and vegetables during postharvest transportation, storage and marketing is an important factor affecting the quality, shelf life and safety of human consumption. Decay caused by plant pathogenic fungi is the main cause of postharvest losses of fruits and vegetables. Fungi are eukaryotic organisms, and the cell wall is essential for the survival of fungal cells. Degradation of the cell wall can cause the fungal cells to lose their osmotic pressure balance, so destroying the integrity of the cell wall has become a potential antifungal measure. β-1,3-glucan is an important antibacterial protein secreted by biocontrol microorganisms, and plants themselves also induce the production of β-1,3-glucanase during the process of resisting fungal infection [53].
β−1、3-glucanaseβ1、分解できるバクテリア3-glucan砂糖フランチャイズの本拠地で細胞壁の原因菌菌の病原性菌類を破って出あるいは、変形もなりたい、の原形質の流出させて病原性キノコ類など胞子萌芽を抑制した。さらに、このプロセスは、真菌の細胞壁フラグメント誘導物質を放出し、植物の免疫誘導を誘導し、間接的に宿主植物におけるフィトアレキシンの蓄積を促進し、耐病性を高めることもできる[54]。生物学的な制御方法β−1、3-glucanase植物のスピピット統制真菌病の予防にも良い。薬剤耐性がなく、他の有益な生物に害を与えることなく目的の病原体のみを標的とし、農薬残留物がなく、毒性や汚染がないという利点があります。したがって探求していくのβの役割−1、果物と野菜類の保護に3-glucanase postharvestや新に緑による実防腐剤β開発−1、3-glucanase潜能开発动向一つ緑色に変り果物や野菜は保存技術
ルーShubaoら[55]βの活動を決定づけた−1、3-glucanase葉や菌類抗菌作用がある。の大豆中その結果、β−1、3-glucanase植物相の活动の全盛を迎える48時間Phytophthora sojaeと接種た後抗菌実験が行われて使用粗β−1、冷静48時間経過し3-glucanase酵素エキス抽出してください発見しβ1、28日、3 -glucanase産軽質油酵素解決策はに対する著明な抑制効果菌糸体成長と胞子萌芽Phytophthora sojae。陳Xiaoyunら[56]βが−1、3-glucanaseは成长にも影响を抑えることが大きいりんごなどの果物のバクテリアと疾患梨とバナナ収获直后、菌類による腐敗post-harvest予防にも良い。この特徴は、熱帯果実の保存と保存に利用できます。[57]がRajninecらか原油β−1、3-glucanase抑制源とbinate毛先から蛋白質である成长にも影响を与えることがRhizoctonia solani、Alternaria solaniとFusarium poae。
オリゴ糖など4.2β−1、3-glucan準備機能
β-1,3-glucan, also known as fucoidan oligosaccharides, is a food functional factor with good biological activity, and has the activity of regulating the body'の免疫、感染に抵抗し、腸内細菌叢のバランスを調節する。利用可能な多糖類やケルプ多糖類を加水分解したβ-1,3-グルカンオリゴ糖は、機能性食品開発における新しいタイプのプレバイオティクスとして利用することができる。さらに、一部の低分子可溶性β-1,3-オリゴ糖は、植物の免疫応答を誘導し、植物の病害抵抗性を向上させる免疫活性化剤として利用できる。また、small-molecule水溶性β−1、3-oligosaccharidesを使用することができる、免疫反応を誘導するための免疫activatorsでの植物を向上した工場病気に抵抗できるものを使いましょうβ−1、3-glucanase hydrolyzesβ−1、3-glucan準備β−1、3-oligosaccharidesは具体的な比較して高いし、それに副産物も少ない。オリゴ糖の製造法として有望であると考えられている。王。[22]がYanxinらかGH55家β−1、3-glucanase (AcGluA) hydrolyze昆布オリゴ糖などオリゴ糖など一連のにいた多糖类や高オリゴ糖などドースは田植えに免疫反応を誘発米爆発を叙位抵抗した。これはβの純度の製品を表して−1、一部な誘引策を提供3-glucanaseに重大なバイオ・コントロール効果はβの届け出−1、3-oligosaccharides。
Li Kuikui etal. [58] cloned and purified a novel β-1,3-glucanase (GcGluE) from Cellulosimicrobium cellulans。基質特異性と加水分解産物を分析した結果、再生可能多糖に対して最も高い加水分解活性を示し、主な加水分解産物は二糖と三糖であった。また、均質化前処理後には、xylan上のgcglueの劣化効率が7.1倍に向上し、一定の適用可能性があります。高版画ら[18]β取得−1、3-glucanase Trichodermaからharzianum、酵素活动198.57まで118 h醗酵U / mLこの酵素の特性に応じて、高潔オリゴ糖など多機能機つのタンパクプロダクトオブザ酵素ための方法β−1、3-glucan成立がβ−1、3-glucan酵素があるアプリケーションオリゴ糖など産業生産企業景気展望の調査。

4.3βの応用−1、3-glucan醸造業界で
ほかに大切な役割を果たしている抗菌オリゴ糖化生产、β−1、3-glucanaseも醸造業て用いられることもある。醸造業界では、大麦がビールの主な原料です。製法期間中、微生物分泌high-molecular-weightβ−1、3-glucan部位空間に反映させ需要によっての発酵液は粘度が増え濾過付近では困難を引き起こした。最終的には、凝集ゲルがビールに形成され、ビールの生産が減少し、醸造コストが上昇する可能性があります。Luリリーのもとでらを続ける。[59]が適切なβ−1、3-glucanaseを加えて発酵過程の内容high-molecular-weight -グルカンが大幅に削減することが可能な溶き具合も発酵さ煮汁を低減リーンの目的達成ビールや濾過過程高める方向に進んでいる。
4.4β−1、3-glucan酵母protoplastsを準備するの
The main chemical component of the yeast cell wall is β-glucan. One type is the relatively abundant β-1,3-glucan, which forms the skeleton of the yeast cell wall. The other type is the less abundant β-1,6-glucan, which fills the space. The key to preparing yeast protoplasts is to break down the insoluble β-1,3-glucan in the cell wall, so β-1,3-glucanase is an important preparation for protoplasts [60]. Duan Huike etal. [61] used the β-1,3-glucanase produced by the Trichoderma strain LE02 to enzymolyze and solubilize the beer yeast glucan. Macromolecular water-soluble yeast glucan can also be obtained by β-1,3-glucanase enzymolysis technology and ultrafiltration separation technology.
4.5β−1、3-glucan生物映画を除去
バイオフィルムは、微生物とその細胞外分泌物から構成される複雑な構造です。サルモネラ菌や緑膿菌(pseudomonas aeruginosa)などの食品中の主要な腐敗細菌は、バイオフィルムを産生し、一般的に使用される消毒剤や抗生物質の殺菌効果を低下させ、食品の安全性のリスクをもたらす。β−1、3-glucanは重要な構成要素であるバイオフィルムの「キャンディダ」というかびや戯曲において重要な役割をecmバイオフィルム。一方、β−1、3-glucanase効果があるという说がありそして、バイオフィルムの艶消し細菌自在に操るを取り除き食品業界ですネットら[62]のCandidaを重く扱う低浓度がβ−1、3-glucanaseが著しく強まっ抗真菌の薬物の作用fluconazole、黒い長方形の区画に菌根をアムホテリシンB。ミッチェルら【63】もは事案の敏感性抗真菌実験するデモがしだいに薬の加水分解が強ければ強いほど向上β−1、3 -グルカンがecmで示すβ−1、3-glucanase生物映画。の解消に効果があるという说があり
4.6βのシナジー効果を−1、3-glucanとchitinase
β——1の3-glucanaseとchitinase効果がある分解β−1、3-glucanや甲壳素peptidoglycanで細胞壁に変えているのです両方の酵素は、植物の害虫や病気に対する防御の広いスペクトル耐性を持っており、化学農薬の使用を減らし、環境汚染を低減することができます。Mauchら[64]発見chitinaseの結合動作及びβ−1、3-glucanase個々人による酵素より抗菌作用があるものにが深いので、2酵素を表すシナジー効果成長の病原性細菌の作用を防ぐのに[65]がCotaらかβのシナジー効果を−1、3-glucanase chitinase抵抗でき大幅の世代にも残るようAlternaria alternataに格納さこのアンジェラは私をプレアだと思ってるこれはβ−1、相乗効果を3-glucanaseとchitinaseは果物と野菜類のpost-harvest抗菌保存、さらに强く持って抗菌力も1個の疲れがよりもアプリケーションのための良い见通しがした。
5結論
β——ので、3-glucanは返す言葉が具体的にはhydrolyzeβ−1、3-glucan、の分野において大切な応募な有望オリゴ糖機能準備、果物や野菜の保存を使えばバイオ医薬品、工場病気に抵抗できるものを使いましょう研究者すでに構造を学び、機能、およびアプリケーション别の家族一連のβ−1、3-glucanases。このような状況の下、焦点後の研究のβ−1、3-glucanases安値に诱导するを得、新規β−1、良好なアプリケーション特性を3-glucanasesに効率的な発酵達成の準備
しかし、比較的複雑であるため,自然β−1、3-glucan基板、既存のβの触媒効率−1、3-glucanasesの異なるタイプ基板をより一層高めなければならないタンパクプロダクトオブザ酵素の一部と不溶性β−1、3-glucan基板は相変らず貧しかった。また、酵素の構造と機能の研究は、酵素の触媒機構の解明、酵素の触媒特性の探索、酵素分子修飾の研究の重要な基盤となっています。複雑性を考慮自然β−1、3-glucan基板とβの多様性−1、3-glucanase家族の意見は学业を発展し食い違いβの異なる基板ステープルおよび触媒メカニズムで−1、3-glucanase家族の基板を明確に認識機構β−1、3-glucanase繁雑-グルカンが分子を模索する必要があるmulti-enzyme触媒組み合わせシステムβ−1、3-glucanaseを達成するために効率よくβアプリケーション−1、3-glucanase。1,3-グルカナーゼは、その効率的な利用のための開発トレンドである。
参考:
[1] kadam s u, tiwari b k, o ' donnell c p .褐藻からのラミナリンの抽出、構造および生体機能活性[j]。国際食品科学技術ジャーナル,2015,50(1):24-31。土井:10.1111 / ijfs.12692。
三好[2] K UEZU K sakurai k, etal。curdlan三重らせんを維持するための新しい水素結合形態の提案[j]。化学&^ a b c d e f g h i(2004年)、916-924頁。土井:10.1002 / cbdv.200490073。
【3】傅雲彬、趙暁明、杜余光。シドラモン多糖類およびその誘導体の生物活性および利用に関する研究[j]。2012年食物科学専攻、33(7):315-319。
[4] shimizu j, tsuchihashi n, kudoh k, et al。食物curdlanは、ラットの盲腸でビフィズス菌の増殖を増加させる[j]。^「bioscience biotechnology and biochemistry, 2001, 65(2): 466-469」。bioscience . 2013年3月6日閲覧。土井:10.1271 / bbb.65.466。
[5] yu yonghua, xu feifei, lin lin, et al。 研究のhypolipidemic効果問題にも進展がオート麦のβ-glucanか[J]。journal of clinical and pathological sciences, 2022, 42(2): 486-491。土井:10.3978 / j.issn.2095-6959.2022.02.034。
[6] davies g, henrissat b .グリコシルヒドロラーゼの構造とメカニズム[j]。^『人事興信録』第5版、853-859頁。土井:10.1016 / S0969 - 2126(01) 00220-9。
[7] ilari a, fiorillo a, angelaccio s, et al。基質の超好熱性塩基からの家族16エンドグルカナーゼの結晶構造 識別か[J]^ febs journal, 2009, 276(4): 1048-1058。土井:10.1111 / j.1742-4658.2008.06848.x。
[8] yuan y, zhang x, zhang h, et al。Degradative GH5β−1、3 1,4-グルカナーゼppbglu5a paenibacillus polymyxaのグルカン KF-1 [J]。プロセス生化学,2020,98: 183-192。土井:10.1016 / j.procbio.2020.08.008。
[9] JAAFAR N R, KHOIR私N m, ismail n f, et al。機能 遠藤characterisation特異性と-β−1、3-glucanase アルカリ性細菌から,bacillus lehensis g1 [j]。酵素 2020年には微生物技術が 140: 109625.
[10] shi p, yao g, yang p, et al。述べ、クローンや防黴活動endo-1の3β-D-glucanase Streptomyces spからS27か[J]。応用微生物学とバイオテクノロジー,2009,85(5):1483-1490。土井:10.1007 / s00253-009-2187-1。
[11] hartl l, gastebois a, aimaniandav, et al。特性化远藤GPI-anchoredβ−1、3-glucanase Eng2 fumigatusれる麹菌か[J]。生物学や遺伝真菌では2011年は、48(2):185-191。土井:10.1016 / j.fgb.2010.06.011。
[12] da silva aires r, steindorff a s, ramada m h s, et al。 27 kdaの生化学的特徴 1、3、-β-D-glucanase誘発型Trichodermaasperellum細胞壁をからRhizoctonia solaniか[J]。炭水化物ポリマー,2012,87(2): 1219-1223。土井:10.1016 / j.carbpol.2011.09.001。
[13] ishida t, fushinobu s, kawai r, et al。グリコシドしてるの家族の水晶构成55β−1、3-glucanase basidiomyceteからPhanerochaetechrysosporiumか[J]。journal of biological chemistry, 2009, 284(15): 10100-10109。
[14] varghese j n, garrett t p, colman p m, et al。三 2工場の次元構造β-glucan endohydrolases创业期基板specificitiesか[J]。ナショナルアカデミー会員 ^「the science of the united states of america, 1994, 91(7): 2785-2789」。science of the united states of america . 2013年9月27日閲覧。
【15位】ロメロ I, FERNANDEZ-CABALLERO C goni o, et al。 1級の機能β−1、3-glucanaseの皮テーブルブドウから 実はか[J]て2008年植物科学、 174(6): 641-648。土井:10.1016 / j.plantsci.2008.03.019。
[16] yu w q, zheng g p, qiu d w, et al。Paenibacillus terrae NK3-4:潜在的なバイオ・コントロールというtr69エージェントへの通知は生産β−1、3-glucanaseか[J]。生物学的制御,2019,129:92-101。土井:10.1016 / j.biocontrol.2018.09.019。
【17位】li c, wen y 彼はY ら浄化 つけたり 小説β−1、から3-glucanaseアルカinflataとその免疫- 効果か[J]強化しています食品化学,2019,290:1-9。土井:10.1016 / j.foodchem.2019.03.131。
[18] gao minjie, yan jiajun, zhao yue, et al。表情を表し thermostableβ−1、3-glucanasefrom Trichoderma harzianumでPichia pastorisで用いるとoligoglucosides分解か[J]。過程 生化学皆に告げ、107:74-82。
[19]張 D した? D VALENTE S et al. 性格は、クローンに固定されたexo-1の表現で、3β-glucanase遺伝子苍真に相対する酵母Pichia guilliermondii株に対するM8灰色カビリンゴか[J]。生物学的制御,2011,59(2):284-293。 土井:10.1016 / j.biocontrol.2011.06.018。
[20] KALYANI D C 名探偵 T, ASPEBORG H et アルhomodimeric細菌エクソ-β−1、3-glucanaseムースない人に微生物由来】構造枠組み酵母エクソに似てβ−1、3 glucanases [J]。酵素微生物技術、2021年まで、143:109723。 土井:10.1016 / j.enzmictec.2020.109723。
[21] yi p, yan q, jiang z, et al。第1のグリコシドてる家遠藤50 -β−1、3-D-glucanase绿脓菌からか[J]。 酵素と微生物技術、2018、108:34-41。土井:10.1016 / j.enzmictec.2017.09.002。
[22] wang yanxin, zhao yuqiang, wang xiaowen, et al。小説の機能特性化laminaripentaose-producingβ−1、3 glucanase MoGluBバイオ・コントロールか[J] Magnaportheの麹は。^「journal of agricultural and food chemistry, 2021, 69(33): 9571-9584」。journal of agricultural and food chemistry . 2018年3月29日閲覧。
[23]成度目。βの表現−1、3-glucanaseでPichia pastoris [D] .^「harbin institute of technology」。harbin institute of technology(2013年). 2013年12月15日閲覧。
[24] feng jianwei, xu shenyuan, feng ruirui, et al。識別および 構造分析し今はなにβ−1、肥料から3-glucanaseか[J]使います。 ^「bioresources and bioprocessing, 2021, 8(1): 102—112」。bioresources and bioprocessing(2018年). 2018年8月1日閲覧。土井:10.1186 / s40643-021-00449-4。
[25]やがてMUHAMMED M T,息子C D、İZGU・f・3次元構造 panomycocinの予測小説エクソβ−1、3-glucanaseから孤立Wickerhamomyces anomalus NCYC 434や計算 治療応用のための熱安定性を高めるための部位特異的変異誘発研究[j]。計算生物学や化学の分野では 80 2019年:270-2777。土井:10.1016 / j.compbiolchem.2019.04.006。
[26] fibriansah g, masuda s, koizumi n, et al。1.3 angstrom水晶構造遠藤小説—β−1、配糖体してると家の3-glucanase 16 alkaliphilic Nocardiopsis sp.株F96か[J]。^ a b c d e f g h i(2007), 69(3): 683-690。
【27】VUONG T V wilson d b . glycoside hydrolases: catalytic base/nucleophile diversity[j]。^「bioengineering and bioengineering, 2010, 107(2): 195-205」。bioengineering and bioengineering(2010年). 2010年10月25日閲覧。土井:10.1002 / bit.22838。
[28] ilari a, fiorillo a, angelaccio s, et al。ファミリーの結晶構造16超好熱性pyrococcus furiosus由来エンドグルカナーゼ基質認識の構造的基盤[j]。^ the febs journal, 2009, 276(4): 1048-1058。土井:10.1111 / j.1742-4658.2008.06848.x。
[29] oda m, inaba s, kamiyan, et al。構造調整やendo-1の熱機械特性化3 -β-glucanase:基板識別機構か[J]を深く理解することが出来る。慶応2年(1866年)2018年BBA-Proteinsプロテオミクス(3):415-425。
[30] jeng w y, wang n c, lin c t, et al。結晶構造 laminarinase触媒紀州藩Thermotoga maritimaと複合したMSB8阻害薬欠かせない残留β−1、3-andβ−1、4-glucan選択か[J]。journal of biological chemistry, 2011, 286(52): 45030-45040。
[31] hong t y, hsiao yy, meng m, et al。の 1.5 angstrom endo-1の構造3β-glucanase Streptomycesからsioyaensis:进化のactive-site構造を1 3、β具体的な-glucan-binding分解か[J]。acta crystallographica section d: structural biology, 2008, 64- 964-970。土井:10.1107 / s0907444908021550。
[32] bleicher l, prates et, gomes t c f, et al。ラミナリナーゼの熱安定性と熱親和性の分子基盤:rhodothermus marinus由来の超熱安定ラミナリナーゼのx線構造と分子動力学シミュレーション[j]。journal of physical chemistry b, 2011, 115(24): 7940-7949。土井:10.1021 / jp200330z。
[33] labourel a, jam m, jeudy a, et al。からのβ-glucanaseZgLamA Zobellia galactanivorans進化し効率曲げ積極的な现场を支える適合藻の劣化laminarinか[J]。日刊生物 化学,2014,289(4):2027-2042。
[34] yang j, xu y q, miyakawa t, et al。海洋細菌ラミナリナーゼによる基質認識と触媒作用の分子基盤[j]。2020適用され、環境微生物学86(23):15。土井:10.1128 / aem.01796-20。
[35] wojtkowiak a, witek k, hennig j, et al。構造のactive-site突然変異第1工場、3β-glucanase复雑なwitholigosaccharideの中で分解か[J]を持つ製品だ。acta crystallographica section d: biological crystallography, 2013, 69, 52-62。土井:10.1107 / s0907444912042175。
[36] RECEVEUR-BRECHO T V CZJトビー M バーレ A et アル、水晶構造の主要なアレルゲン遠藤1.45-A解像度で—β−1、バナナのような3-glucanaseがいくつあるとしてlatex-fruit ?シンドロームか[J]があった。^ a b c d e f g h i (2006), pp . 235-242。
[37] unfried f, becker s, robb c s, et al。藻類ブルーム発生時に海洋細菌に競争優位性を与える適応機構[j]。2018年ISMEジャーナル 12(12): 2894-2906。土井:10.1038 / s41396-018-0243-5。
[38] takashima t, taku t, yamanaka t, et al。水晶CJP38の二重構造生物化学特性化は1种のβ−1、3-glucanase花粉スギジャポニカか[J]アレルゲンした。分子免疫学,2019,116:19 -207。
[39] wu h m, liu s w, hsu m t, et al。構造当てはめよ行动すれば、环境に不可欠な残留でGH-64酵素laminaripentaose-producingβ−1、3-glucanaseか[J]。journal of biological chemistry, 2009, 284(39): 26708-26715。
[40] qin zhen, yang dong, you xin, et al。識別機構triple-helicalβ−1、によって3-glucanβ−1、3-glucanaseか[J]。chemical communications, 2017, 53(67): 9368-9371。土井:10.1039 / c7cc03330c。
[41] GHOSH R, CHAKRABARTI C 水晶 ソーマチン様タンパク質np24-iの構造解析[j]。^『官報』第2828号、大正8年(1920年)8月8日。 土井:10.1007 / s00425-008-0790-5。
[42] HENRISSAT B GARRON M Lを有する。どう a グリコシドヒドロラーゼはヘリカルポリグルカンを認識する[j]。構造、2017年、25 (9): 1319-1321。土井:10.1016 / j.str.2017.08.004。
[43]クマールはKので コレイアm a s ピレスV M R, et アル小説 洞察βの劣化1、3-glucansby cellulosome ファミリーの構造と機能の研究によって明らかにされたclostridium thermocellumの81グリコシド加水分解酵素[j]。国際学術誌「ネイチャ・フォトニックス 生物学的高分子の,2018,117:890-901。土井:10.1016 / j.ijbiomac.2018.06.003。
[44] zhou peng, chen zhongzhou, yan qiaojuan, et al。の構成配糖体してる家遠藤81 -β−1、3-glucanaseか[J]。acta crystallographica section d: structural biology, 2013, 69: 2027-2038。土井:10.1107 / s090744491301799x。
[45]馬雲Junwen、 周秦ジン 鵬 ら構造洞察基板識別、触媒菌類メカニズムを配糖体してる家81β−1、3-glucanaseか[J]。酵素と微生物の技術,2022,153:109948。[46] pluvinage b, fillo a, massel p, et al。構造分析家の81配糖体してると、グローバリゼーションに対する認識に飛び火β−1、3 -グルカン四進法構造か[J]です。^ a b c d e f g h i(2017年9月25日).「what ' s in ?土井:10.1016 / j.str.2017.06.019。
[47] bianchetti c m, takasukat e, deutsch s, et al。グリコシド加水分解酵素ファミリーの活性部位とラミナリン結合55[j]。journal of biological chemistry, 2015, 290(19): 11819-11832。土井:10.1074 / jbc。M114.623579。
[48] papageorgiou a c, 陳 J 李 d .水晶 構造と生物的側面を配糖体してる家と55β−1、3からglucanase Chaetomium thermophilumか[J]。 biochimica et biophysica acta-proteins and proteomics, 2017, 1865(8): 1030-1038。 土井:10.1016 / j.bbapap.2017.05.002。
[49] jia x, wang c, du x, et al。家族が小説配糖体してるとなcurdlanの特定の加水分解128β−1、3-endoglucanase carbohydrate-bindingモジュールか[J]を備えている。炭水化物ポリマ-,2021年253:117276-117286。
[50] santos c r, costa p, vieira p s, et al。構造洞察β−1、3-glucanだろ配糖体してると家族にか[J]。nature chemical biology, 2020, 16(8): 920-929。土井:10.1038 / s41589-020 - 0554-5。
[51] gastebois a, aimanianda v, BACHELLIER-BASSI Sら小説家の孫タンパク質に属するβ-(1、3、)-glucan-modifying酵素の形態形成菌類関与か[J]ですjournal of biological chemistry, 2013, 288(19): 13387-13396。
[52] dejean g, tamura k, cabrera a, et al。シナジー細胞の表面やglycosidases glycan-bindingたんぱく質利用への特定βBacteroidesため経口摂取(1、3、)-glucansことか[J]。mbio, 2020, 11(2): 1-21。
[53] yan f, ye x l, li c h, et al。分離精製遺伝子クローニング bacillus amyloliquefaciensの抗真菌タンパク質の発現 mg - 3 [j]。 食品 化学 2 0 2 1 3:4 9 7 . 約数の和は1,0。1 0 1 6 / j.foodchem.2021.129130。
[54] FESEL P H a ZUCCAROβ-Glucan:菌類細胞壁を重要な成分するあやしく、もっとも難しいMAMPin植物か[J]。生物学や遺伝真菌では2016年90:53-60。土井:10.1016 / j.fgb.2015.12.004。
[55] lou shubao,彭東軍,王輝。大豆の静菌活動β−1、3-glucanaseか[J]。黒竜江省八一農業大学紀要,2008(3):27-29。
[56] chen xiaoyun, li jianbin, lin ying, et al。βの応用−1、3-glucanaseとchitinaseか[J]の熱帯果実を保存しようとすることです。食品産業科学技術,2008(5):294-296。
[57] rajninec m, fratrikova m, boszoradova e, et al。基本β−1、3-glucanase毛先からbinata展示物を防黴潜在遺伝子組み換えタバコ植物か[J]。植物は2021年まで 10(8日): 1747-1762。土井:10.3390 / plants10081747。
[58] li kuikui, chen wei, wang wenxia, et al。小説遠藤で粉末curdlanの劣化が有効だとβ−1、3-glucanaseか[J]。炭水化物ポリマ-,2018 201:122-130。土井:10.1016 / j.carbpol.2018.08.048。
[59] lv lili, wang ruibin, wang jialin, et al。高効率の効果β-glucanaseか[J]汁の濾過率。^ a b c d e f g h『科学と技術』、2010年、75-77頁。土井:10.13746 / j.njkj.2010.03.028。
[60]林開江、阮麗娟、王龍英。セルラーゼを用いた酵母プロトプラストの作製に関する研究[j]。^「science and technology bulletin」。science and technology bulletin . (1996) . pp . 12 .(2): 118-121.(英語)
【61】段慧可、熊山伯、劉海美。 酵母の酵素solubilizationβ−1、3-glucanと製品分析か[J]。2008年食物科学専攻、29(1):185-189。
[62] nett j, lincoln l, marchillo k, et al。Putativeβの役割−1、「キャンディダ」というかび3 glucansバイオフィルム抵抗か[J]。抗菌の agents and chemotherapy, 2007年51(2): 510-520。土井:10.1128 / aac.01056-06。
[63] mitchell k f, taff h t, cuevas ma, et al。マトリックスβの役割−1、3 -グルカン防黴の抵抗のnon-albicans Candida生体膜か[J]。 ^ a b c d e「antimicrobial agents and chemotherapy, 2013」。antimicrobial agents and chemotherapy(2013年). 2018年3月25日閲覧。 土井:10.1128 / aac.02378-12。
[64] mauch f、mauch-mani b、boller t .エンドウ組織における抗真菌ヒドロラーゼ:ii。抑制chitinaseの組み合わせによる菌類成長β−1、3-glucanaseか[J]。植物生理学 1988年、88(3):936-942。
[65] COTA I E TRONCOSO -ROJAS R, ソテロ-MUNDO R, ら Chitinaseとβ−1、3-glucanase 酵素 活動 in alternariaによる感染に対する応答alternataは2つで評価されました さまざまなトマト果実品種の開発段階[j]。 Scientia Horticulturae、 2007, 112(1面) 42。


 英語
英語 フランス
フランス スペイン
スペイン ロシア
ロシア 韓国
韓国 日本
日本




