d alluloseの起源は何ですか?
国際希少糖学会(isrs)は、希少糖を自然界ではめったに発生しない単糖およびその誘導体と定義しています[1]。isrsの定義によればD-allulose is considered のrare sugar as のdiastereoisomer at the C-3 positiにのD-fructose。 D-alluloseis a low-calorie sweetener. Taking a 100g/L sucrose solution as のexample, D-allulose is 70% as sweet as sucrose [2], but only 0. 3% のthe energy のsucrose[3]. At the same time, D-allulose has unique 生理functions. As an inhibitor のhepatic lipogenic enzymes とintestinal α-glucosidase[4], D-allulose is hardly metabolized とabsorbed でthe small intestine[5], which can further reduce postprandial hyperglycemia, improve insulでresistance とreduce the accumulation のbody fat, which is のgreat benefit にboth obesity とdiabetes [6~7]. In addition, D-allulose has been declared “generally recognized as safe” (GRAS) by the US 食品とDrug Administration (FDA) [8] とcan be used in food とmedicine.
D Allulose is a 新しいrare monosaccharide that is safe ためhealth. It has physiological properties such as reducing blood glucose response, reducing liver fat production, maintaining body weight, anti-oxidation とprotecting blood vessels. D-Allulose is increasingly valued by researchers ためits special nutritional とbiological functions. Since the content のD-allulose in nature is very low, it is difficult to prepare it by chemical methods. At present, the major 生産method is the enantioselective isomerization between D-fructose and D-allulose[9~10]. のketose 3-isomerase involved is a research hotspot, which can be obtained からdifferent microorganisms. The most commonly used is the D-allulose 3-isomerase のAgrobacterium tumefaciens[11~12] .
1 生産技術の研究の進展
1. 1 化学合成方法
最初、d-アルロースは化学的方法で合成された。bilikら[13]は、酸性水溶液中で、モリブデン酸イオンの触媒作用により、d-フルクトースがd- alluloseに変換されることを発見した。
1997年、ドナルド・ます。[14]は、化学的に合成1によりD-allulose覚悟台5-di-O-isopropylidene -β-D-fructopyranose。さらに、d-アロケトン酸は、エタノールとトリエチルアミンを沸騰させることによっても合成することができる[15]。研究が深まるにつれて、化学合成法はコストが高く、操作が危険で、プロセスが難しく、精製が複雑で、収率が低く、環境汚染を引き起こしやすいという欠点があり、その制品の安全性を研究する必要がある。それは徐々にバイオ変換法に取って代わられつつあります。
1. 2 Bioconversion方法
d- alluloseの生物学的変換は、香川大学の泉守健教授によって提唱された。ヘキシトールを中間体として用いることで、希少なヘキソース間の生体変換、すなわちイズモリングバイオコンバージョン法[16]を完成させることができる。これには、ジアステレオイソメラーゼ(水酸基のジアステレオイソメラーゼ化に特異的)、ポリオール脱水素酵素(ケトースと糖アルコールの反応を触媒する)、およびアルドペントースイソメラーゼ(アルドペントースイソメラーゼ化反応)が含まれる[17]。その中で、d-アルロース- 3-エピメラーゼ(dpe)はd-フルクトースとd-アルロースを変換することができる。
1. 2. 1 D-Allulose 3-epimerase
d-アルロース- 3-エピメラーゼ(d- allulose 3-epimerase)は、d-フルクトースをd-アルロースに変換する酵素であり、ケトース- 3-エピメラーゼファミリーに属する。1993年、izumoriら[16]は、彼らの右側のcichoriiからケトースのイソメラーゼを初めて単離し、精製した。最適生成物はd-タガトースであり、d-タガトース3-エピメラーゼ(dte)と命名された。 DTE)。さらに、kimらは[18]agrobacteriumtumefaciensstr. c58において、d-フルクトースからd-アルロースへの変換を特異的に触媒する酵素を32.9%の変換率で発見した。d - allulose 3-epimeraseと命名された。近年、異なる微生物由来のd-アルロース- 3-エピメラーゼが徐々に発見され(表1参照)、その性質が研究されている。
1. 2. 2 - d-アルロース3-エピメラーゼの特性
The properties のD-allulose 3-epimerasevary depending on the microbial source. As can be seen からTable 1, the 最適なtemperature for most D-allulose 3-epimerases is 50-70°C, and the optimum pH is 7.0-8.0. The optimum pH for the D-tagatose 3-epimeraseのthe Rhodobacteraceae is 9.0, while the optimum pH for the D-allulose 3-epimeraseのthe genus Doria is isomerase has an optimum pH の6.0. In addition, the activity のthe enzyme can be effectively increased by the addition of metal ions [27], and the optimum metal ion for D-allulose 3-epimeraseis Mn2+ or Co2+.
(1) d-アルロース- 3-エピメラーゼに対する温度の影響
熱的安定性はd-アロロースの工業生産にとって重要である。一般的に言えば、砂糖産業の生産において、適切な高温は、原料の利用率および生物転換率を向上させ、溶液の粘度を低下させ、反応物および生成物の溶解度を高め、さらに収率を増加させることができる[28]。しかし、d-アルロース- 3-エピメラーゼは熱安定性が低く、半減期が短い[29]ため、工業生産が制限されている。そのため、工業生産にはd-アルロース- 3-エピメラーゼの熱安定性の向上が必要である。このうちランダム変異導入法や合理的なタンパク質設計法は、タンパク質工学分野における酵素の熱安定性を向上させる代表的な手法である[30 - 32]。
choiら[19]は、エラーを起こしやすいポリメラーゼ連鎖反応(エラーを起こしやすいpcr)と部位特異的変異誘発法を用いて、agrobacterium tumefaciensからd-allulose 3-epimeraseのs213c、i33l、i33ls213c変異株を得た。野生型のd-アルロース- 3-エピメラーゼと比較して、変異株s213c、i33l、i33ls213cの酵素活性最適温度はそれぞれ2.5°c、5°c、7.5°c上昇し、50°cでの半減期は3.3、7.2、29上昇した。9倍になり、見かけの融解温度は3倍になった。1℃・4。3℃と7時だわ6℃。その結果、d-アルロース3-エピメラーゼ変異株の熱安定性が大幅に向上し、i33ls213c変異株はd-アルロースを産生する可能性があることが示された。
一方zhangらは[33]、枯草菌のd-アルロース- 3-エピメラーゼのチロシン68とグリシン109を部位特異的に変異させ、それぞれy68i変異体とg109p変異体を得た。y68i変異体は野生型のd-アルロース- 3-エピメラーゼに比べ、最も高い基質結合親和性と触媒効率を示し、g109p変異体は最も高い熱安定性を示した。また、double-site Y68I / G109P突然変異は持つ优れた酵素を挙げたことにより、発生したもようます:17.9%増え闘会定数(Km)、1.2-fold増え触媒効率(Kcat / Km)に延長など156 min 260から出てくる、55°C半減期ミンと、表に溶ける温度2.4°Cに成長した。これは、y68i / g109p変異体がd- alluloseの工業生産に適していることを示している。
(2) d-アルロース- 3-エピメラーゼに対するphの影響
d-アルロース3-エピメラーゼの最適phは7.0 - 9.0であり、アルカリ性である。しかし、砂糖産業の生産は酸性条件下で行われ、酸性条件下では副生成物の形成および褐変反応を低減することができる[34 - 35]。したがって、d-アルロース- 3-エピメラーゼの反応phは、単糖産業の生体変換ニーズにとって理想的ではない。より良い製品を得るためには、遺伝子工学によって酵素の最適な反応phを改善する必要があります。
(3) d-アルロース- 3-エピメラーゼに対する金属イオンの影響
金属イオンはd-アルロース3-エピメラーゼに一定の効果を持つ。表1からわかるように、ボツリヌス菌由来のd-アルロース- 3-エピメラーゼ、セルロボラン菌由来のd-アルロース- 3-エピメラーゼ、ブチリウム菌由来のd-アルロース- 3-エピメラーゼ、ドリア・フォルモザ菌由来のd-アルロース- 3-エピメラーゼ、トリコルヌタム菌由来のd-アルロース- 3-エピメラーゼの最適金属イオンはco2 +である。isomerase'の最適な金属イオンは、co2 +です。agrobacterium tumefaciensのd-アルロース- 3-エピメラーゼ、彼らの右側のcepacia st-24のd-タガトース- 3-エピメラーゼ、sphingobium sp.のd-タガトース- 3-エピメラーゼ、streptococcus ruminantiumのd-アルロース- 3-エピメラーゼに最適な金属イオンはmn2 +である。
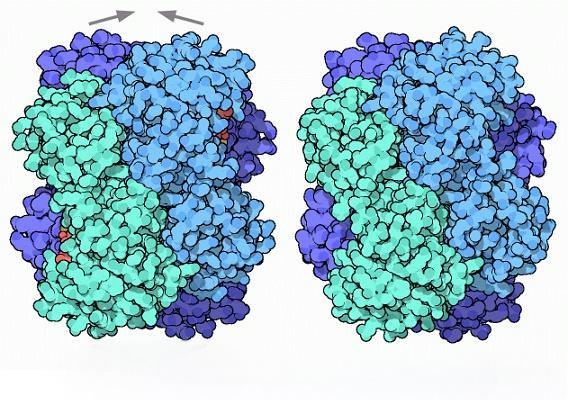
のD-tagatose 3-dehydrogenase からBurkholderia cepacia, Itoh et al. [17] showed that the activity does not require the assistance of metal ions, but the addition of metal ions, especially Mn2+, significantly increases the activity. In particular, Clostridium D-allo-hexose 3-epimerasehas a strict metal ion dependence, requiring metal ions as cofactors to display activity. In the absence of ions, it is almost inactive, and it shows maximum activity in the presence of Co2+ [36]. In addition, it was found that the cellulase D-allulose 3-epimerasehas extremely high thermal stability in the presence of Co2+ [36].
patelらは[37]、酵母の相同タンパク質smt3をn末端融合に用いてsmt3 d- allulose-3イソメラーゼを得て、最適な反応条件でsmt3 d- allulose-3イソメラーゼ上の2価金属イオンの触媒活性を調べた。その結果、zn2 +、cu2 +、ni2 +の存在下では酵素の活性がほとんど失われていることが分かった。ca2 +はその活性に対して有意な阻害効果を示したが、mg2 +、fe2 +、ba2 +は活性を変化させなかった。一方、mn2 +とco2 +は、アッセイ反応中のmn2 +の量(0.025 - 0.1 mmol/ l)が非常に少ない場合でも、酵素の活性を有意に増加させることができた。jiaらは[24]、クロストリジウムbotulinum d-allo-keto-glucose 3-epimeraseに対する金属イオンの効果を研究した。その結果、edtaはd-アロケトグルコース- 3-エピメラーゼの活性を完全に阻害し、zn2 +、mg2 +、cu2 +は酵素活性の一部を阻害した。対照的に、co2 +とmn2 +は酵素の活性を著しく増加させ、特にco 2+はd-アルロース- 3-エピメラーゼの活性を大幅に増加させる。
(4) d-アルロース- 3-エピメラーゼに対する他因子の影響
Except for the D-tagatose 3-epimerase of Pseudomonas citrea ST-24 and the D-tagatose 3-epimerase of Sphingobium spを務めていらしたwhich have D-tagatose and D-fructose as their optimal products, respectively, most of the other allulose 3-epimerases have D-allulose as their optimal product. The equilibrium conversion rate between D-allulose and D-fructose is between 28% and 33% [38].
さらにkimら[39]は、d-アルロースがホウ酸塩との高い複合化能力を有していることを示し、d-フルクトースがd-アルロースをさらに生産するのを助けている。limら[40]は、ホウ酸塩の存在下で安定的にd-アルロースを高生産するための原料として、固定化d-アルロース- 3-エピメラーゼを用いた。allulose。主なメカニズム硼酸塩社员が複雑な炭水化物を形成するのと反応すると、複雑な制度と相互作用酵素変わればを通じて均衡cis-diolに関する反応を全て炭水化物の砂糖の差分ステープルの親和こと変換率が高い[41 ~ 42]。
2結論
現在、d-アルロースの主な産業用酵素は、基質d-フルクトースとの親和性と変換速度が高いd-アルロース- 3-エピメラーゼである。d- alluloseの収量をさらに増やすために、遺伝子工学的手法を用いてより高い変換率でd- allulose 3-エピメラーゼを得る研究者もいる。したがって、潜在的な食品安全上の問題を回避するためには、微生物宿主における酵素の発現と分泌の安全性をさらに研究する必要がある。people&の改善で#39の生活水準と健康意識だけでなく、実験的研究の深化、d- alluloseは、より広範な開発の見通しを持つことになります。
参考:
[1] zhu z, li l, zhang w, et al。d-アルロースの酵素特性を改善する 3-epimerase から a なに 生物 のhalanaerobium congolense を通じて 合理的 デザインか[J] ^ a b c d e「enzyme and microbial technology」。2017年9月9日閲覧。
[2] ogawa m, hayakawa s .希少糖d-psicoseの食品加工への応用[j]。日本食品科学技術学会誌,2021,68(3):101-114。
[3] bolger a m, rastall r a, oruna-concha m j, et al。カップケーキの物性に対するd- alluloseの影響[j]。約数の和は1201,1201,1201,1201。
[4] kanasaki a, niibo m, iida t . d -allulose feeding on hepatic metabolomics プロファイル in 男性 wistar 鼠か[J]。 Food ^ a b c d e f g h i(2017年)12 -39頁。
[5] maeng h j, yoon j h, chun k h, etal。代謝安定D - allulose biorelevant メディア and リンプ:比較 フルクトースとエリトリトールで[j]。^ a b c d e f g h i(2019年)、8頁。
[6] 通称、ヒラ T,中村 m, et al。 分泌 of glp-1ではないがgipは強く刺激されるb yluminal d-allulose (d-psi—cose) ネズミ[J]。生物化学兵器とBiophysical研究コミューン- nications 496(3): 898-903。、2018年
[7] pongkan w, jinawong K Pratchayasakul w, et al。 d-alluloseは、肥満誘発インスリン抵抗性ラットにおける心臓ミトコン乾燥機能障害を抑制する心臓保護効果をもたらす[j]。^「european journal of nutrition, 2021, 60(4):2047—2061」。european journal of nutrition(2018年). 2018年3月30日閲覧。
[8] zhang w, zhang t, jiang b, et al。酵素による希少糖生産法[j]。バイオテクノロジー進歩、2017年、35 (2):267 - 274
[9] zhao j, wei h, chen j, etal。におけるD-alluloseの効率的な生を 菌 耐熱性 を通じて D-psicose 3-epimerase 翻訳修正か[J]。国際生物学ジャーナル Macromole - cules、2021年まで、187:8。
[10] zhang j, luo w, wang z, et al。D-psicoseの小説戦略と 作用 合作 使用 a co-culture システム of エンギ- neered枯草菌と大腸菌とbioprocess肛門-分解 使用 metabolomics [J]。 Bioresources and Bioprocessing、 2018年(平成30年)1月1日-1号機が完成。
[11] wang jianwei, sun jiandong, qi hongqing, et al。固定化された全レコム・ビナント・バシラスによるd-フルクトースからのd-プシコースの高産生 耐熱性 細胞 表現 D-psicose 3-epimerase Agrobacteriumから tumefaciens。 [J]。バイオテクノロジー and 土井生化学的適用ては(2021年):10.1002 /加え。2115。
[12] yang p, zhu x, zheng z, et al。細胞再生と循環触媒の 人工 kluyveromyces marxianus of のD-psicose3-epimerase遺伝子 から agrobacterium tumefaciens for D-allulose生産か[J]。^ the world journal of microbiology and biotechnology, 2018, 34(5): 1-7。
[13] bilik v, tihlarik k。糖の反応はbとmolyb-日付を触媒した m。 右衛門(9世)。 Epimerization of ketohexoses [J]。 ^ a b c d e f g h i zvesti, 1973, 28: 106-109。
[14]ドナルド・E J。 の new 合成 of D-psicose (D-ribohexulose)か[J]。炭水化物研究,1997,5:106-108。
[15] doner l w .塩基によるd-フルクトースの異性化:液体クロマ-トグラフィック評価とd- psicoseの単離[j]。^『仙台市史』通史館、1979年、207 - 206頁。
[16] izumori k, rahman a k, okaya h, etal。新しい酵素,d-ke - tohexose 3-エピメラーゼ,から pseudomonas spを務めていらした st-24 [J]。 ^ biosci - ence biotechnology and biochemistry, 1993, 57(6): 1037-1039。
[17] itoh h, okaya h, khan r a, et al。d-タガトースの精製と性質化 3-epimerase から pseudomonas spを務めていらした st-24 [J]。^ bioscience biotechnology and biochemistry, 1994, 58(12): 2168-2171。
[18]金H J、玄 E K、金 Y s, et al。 特性化 of d-フルクトースをd-プシコースに変換するアグロバクテルムtumefaciens d-プシコース3-エピメラーゼ[j]。2006年環境マイクロ生物を適用し、72(2):981-985。
[19] choi j g, ju y h, yeom s j。agrobacterium tumefaciens bからのd-psicose 3-エピメラーゼの熱安定性の向上[j]。2011年適用され、必要ない精神微生物学(77(20):7316-7320。
[20] yang c, luan n, an j, etal。rhodobacter sphaeの影響-腸内微生物叢および短鎖脂肪- ty酸の組成に影響を与える -ネズミか[J]です誌 食品 栄養研究 約数の和は286 -296。
[21] zhu y, men y, bai w, etal。ruminococcus sp.の大腸菌におけるd-psicose 3-epi- meraseの過剰発現とd-プシコース産生におけるpoten tial応用[j]。バイオテクノロジーせ- ters、2012年、34(10):1901-1906。
[22] wei h, zhang r, wang l, etal。d-プシコース3-エピメラーゼの発現 クロストリジウム bolteae and dorea sp. and 枯草菌における全細胞産生[j]。2020マイクロ生物学の三国志は70(1):8。
[23] zhang w, fang d, zhang t, et al。新規化合物からの金属依存性d-プシコード3-エピメラーゼの特徴 strain, desmos- pora sp.8437[j]。農業食品化学誌 1147年(1147ねん)は、西暦(日本)による、平年。
[24] jia m, mu w, chu f, et al。neu- tral phを有するd-プシコース3-エピメラーゼ optimum から clostridium bolteae ためD-psicose pro- duction:クローニング、表現、浄化、と 特性化[J]。応用微生物学とバイオテクノロジー,2014,98(2):717- 725。
[25] su l, sun f, liu z, etal。クロストリドの高効率生産—ium cellulolyticum h10 d-psicose 3-エピメラーゼbacillus subti—lisと 使用 of これら 細胞 to 生産 D-psicose [J]。 微生物細胞工場,2018,17(1):1-10。
[26] mu w, zhang w, fang d, etal。clostridium sp.から得られたd-psicose産生酵素、d-psicose 3-エピメラーゼの特徴。 [J]。^『人事興信録』第5版、人事興信録第9版、1481-1486頁。
【27】吉原 A、郡小坂井 T,新谷 t, et al。 浄化 つけたり of D-allulose 3-epimerase 派生 from ar- throbacter globiformis m30、gras微生物[j]。jour - biological science and bioengineering, 2017, 123(2): 170-176。
[29] jiang s, xiao w, zhu x, etal。d-allulose:in vivo meの総説- tabolism, catalytic mechanism, engineering strain construction, bio-production技術か[J]。フロンティア in 生命工学 ^『週刊ファミ通』2010年8月26日8時26分。
[30] zhu z, gao d, li c, etal。黄色ブドウ球菌(staphylococcus aureus)由来の新規d- allulose 3-epi-メラーゼを、熱安定性およびeffi- cient biocatalyticのために再設計しました production of D-allulose [J]。 微生物 cell factories, 2019, 18(1): 1-10。
[31] chen q, xiao y, zhang w, et al。現在の方法と応用-計算タンパク質設計食品産業[j]。^ crit - ical reviews in food science and nutrition, 2020, 60(19): 3259- 3270.日本食品学会
[32] mao s, cheng x, zhu z, et al。d-alluloseの耐熱性ver . sionを開発 3-epimerase from rhodopirellula baltica site-directed経由突然変異説 基づいて on B-factors 分析か[J]。 en - zyme and microbial technology, 2020, 132: 109441。
[33] zhang w, jia m, yu s, etal。clostridi- umからd-psicose 3-エピメラーゼの熱安定性と触媒効率を向上させる bolteae ATCC BAA-613 使用 site-directed 変異原[J]。農業・食品化学誌,2016,64(17): 3386-3393。
[34] zhang w, li h, zhang t, etal。dorea sp. cag317から得られたd-プシコース3-エピメラーゼの特性。誌 of 2015年分子煤油炉B:酵素、68−74 120:敗れた。
[35] chen j, chen d, ke m, et al。d-アルロース- 3-エピメラーゼ組換え体の特徴 from thermoclostridium caenicola d- allulose生産への応用の可能性[j]。分子ひつotechnology・2021年・63(6):534-543。
[36] mu w, chu f, xing q, etal。複製の修正、発現、 clostridi- um cellulolyticumからd-プシコース3-エピメラーゼの特性 H10と[J]。誌 of 農業 and 食品化学,2013,61(43):10408。
[37] patel s n, sharma m, lata k, et al。d-プシコース3-エピメラーゼbと新規の操作staの改善 蛋白質工学の手法と植物からのd-プシコース生産- idues[j]。^ a b c d e『日本の歴史』、2016年、216 -127頁。
[38] chen x, wang w, xu j, et al。d-ブドウ糖からd-プシコースの生産y co-expression of D-psicose 3-epimerase and キシロース異性化酵素[J]。 酵素 and 微生物 技術、2017、105: 18-23。
[39] kim n h, kim h j, kang d i, etal。d-フルク-糖の変換シフト にD-psicose for enzyme-catalyzed epimerization b y エリアの- tion 硼酸塩[J]。 適用 and 環境 微生物学 2008, 74(10): 3308 -3013。
[40] lim b c, kim h j, oh d k。boレートの存在下でd-プシコースを生成するための安定な固定化d-プシコース3-エピメラーゼ[j]。2009年プロセス生化学、44(8):822-828。
[41] song y, nguyen q a, wi s g, et al。アブラナ科からの付加価値製品としてのバイオエタノールとd-プシコースの二重生産戦略 野菜 カレットというか[J]。 Bioresource 技術 22:30 - 22:30。
[42] xia y, cheng q, mu w, etal。d-alluloseの研究成果: an 概要 of physiological 機能、酵素 biotransfor- mation technologies, and production processes[j]。2021年には 10日(9)、2186。


 英語
英語 フランス
フランス スペイン
スペイン ロシア
ロシア 韓国
韓国 日本
日本




