人参エキスの健康効果はどれらがありますか?
人参 is a traditional precious Chinese medicinal herb with a complex chemical composition and a wide range のbiological activities. With the advancement of modern separation and analysis techniques, the chemical composition of ginseng has been further elucidated. Ginsenosides are considered to be the maでactive substances in ginseng, accounting for about 4%. According to the different saponins, ginsenosides are divided into protopanaxadiol saponins, protopanaxatriol saponins and oleanolic acid saponins. So far, more than 40 ginsenoside monomers have been isolated and identified. In recent years, the pharmacological effects and mechanisms of ginsenosides have been widely studied. This article reviews the progress of pharmacological research on ginsenosides at home and abroad.

1ギンセノシドの抗腫瘍効果
この30年間、高麗人参とその近縁種の抗腫瘍活性に関する研究は深化し続け、ジンセノシドrg3、rg1、rh1、rh2、rb1など、さまざまな抗腫瘍活性成分が発見された。この材料、一定の临床応用潜在腫瘍細胞ののアポトーシスを推し進め、腫瘍細胞の拡散抑制の侵略や腫瘍細胞転移抑制、腫瘍血管新生抑制反転開始腫瘍の抵抗影響シグナル変換腫瘍に係わる遺伝子颜に腫瘍放射線患者免疫の極大化を図る。特に、腫瘍患者の放射線療法および化学療法の副作用を低減し、治療薬に対する腫瘍細胞の感受性を高めることに特に顕著である。
金姸兒選手ら[1、2]がginsenoside Rb1規模でナチュラルキラーさを大きく向上させ(NK)セル機能腫瘍壊死因子(TNF) -αコンテンツ時の効果を探る書物ginsenosideアポトーシスをRb1と5-fluorouracilに関連してRg1脾リンパ球のラットS180 tumor-bearingからかかった酢酸デキサメタゾン行為が5-フルオロウラシルの阻害効果に拮抗(p <0.05)。jie jianらは[3]、がん原遺伝子pim-3の発現およびリン酸化不良タンパク質pbad (ser112)および(ser136)の発現に対するギンセノシドrg3の効果を研究した。ギンセノシドrg3は、膵臓癌のpanc-1細胞においてpim-3とリン酸化不良タンパク質の発現を低下させ、それによってpanc-1細胞の増殖を阻害し、アポトーシスを誘導することを発見した。
Yoo JH et al. [4]studied the inhibitory effect of ginsenoside KG-135 ヒト前立腺がん細胞株du145、pc-3および腫瘍を持つマウスの増殖。その結果、kg-135はg1期に細胞周期を停止させることでdu145細胞とpc-3細胞の増殖を著しく抑制することが明らかになりました。免疫組織化学的分析により、kg-135は増殖細胞核抗原(pcna)の発現を低下させることが示された。その作用機序には、細胞周期の阻害とtnfrsf25およびadra2a遺伝子の発現調節が関与している可能性がある。liu tgら[5]は、ギンセノシドrg3とゲムシタビンの併用による血管新生とマウス肺がんの阻害を研究した。その結果、肺がんマウスの腫瘍の成長を阻害し、生存率と生活の質を改善しただけでなく、腫瘍の壊死を有意に促進し、血液と腫瘍組織の血管内皮増殖因子(vegf)の発現を阻害した。李SYらをしているからです[6]ginsenoside Rdの抑制効果结肠ガン細胞HT29 ginsenoside Rdが14規制の斡旋のタンパク質(Stathmin 1は、たんぱく质microtubule-associated RP / EB家族・Stratifin)とapoptosis-relatedと密接に関係しての蛋白质(剤游离類似度ρGDPにTropomyosinは1、Annexin 5)、ギンセノサイドrdによる大腸がん細胞ht29の増殖阻害は、上記のタンパク質と関係していると推測される。
2 anti-Alzheimer's病(ad)ギンセノシドの効果
AD is a neurodegenerative disease that mainly occurs in early old age and old age. The main clinical manifestations of AD patients are memory loss and 認知impairment. Ginsenosides, the main active ingredient in ginseng, have anti-aging, memory-enhancing and geriatric disease-treating properties. They can increase the amount of acetylcholine (Ach) in the brain, increase the number of cholinergic nerve M receptors, and have a bidirectional regulatory effect on the central nervous system. They also have anti-inflammatory and antioxidant properties, protect nerve cells, reduce their apoptosis, and promote the synthesis of nucleic acids and proteins. In recent years, ginsenoside treatment of AD has been receiving increasing attention. Its mechanism is mainly related to promoting the activity of β-secretase and γ-secretase, which promote the formation of β-amyloid (Aβ), as well as protein phosphatase 2A, anti-oxidation and elimination of free radicals.
Wang YH et al. [7] studied the inhibitory effect of ginsenoside Rg1 on β-secretase activity and its protective effect on Aβ-induced cytotoxicity in PC12 cells in vitro. The results showed that ginsenoside Rg1 can inhibit β-secretase activity and protect PC12 cells from the damage caused by Aβ, such as lactate dehydrogenase (LDH) release, nitric oxide (NO) release, reactive oxygen species (ROS) production, lipid peroxidation, intracellular calcium elevation, and apoptosis. Li Yongkun et al. [8] established an animal model of Tau protein hyperphosphorylation by injecting Okadaic acid into the dorsal hippocampus, and investigated whether ginsenoside Rb1 has a relieving effect on Tau protein hyperphosphorylation.
その結果、ギンセノシドrb1は、ラット海馬神経細胞のオカダイク酸によって誘導されるタウタンパク質の過リン酸化を減少させることができ、そのメカニズムはタンパク質ホスファターゼ2 aの活性増加に関連している可能性があることが示された。石はYQら。[9]の効果を学びginsenoside Rg1宣誓証言β仮面を認知能力で急速な高齢化のネズミ(SAMP8)の後長期政権がginsenoside Rg1、SAMP8ネズミ海馬β尋問格段に減るだろうた大きく水準の低いPKARIIα短期記憶を司る海馬に、phosphorylated循環アデノシン一リン酸のレベル応答素子結合タンパク質(CREB)とneurotrophic神経栄養因子(物質)を大幅に上回っている。さらに、samp8マウスの学習能力と記憶能力も同様に向上した。壮さくらら。[10]ginsenosideの効果を調査Rg2学習と記憶能力に合わせてし老いぼれ看板(SP)布陣で臨んだ広告誘発型モデル鼠β25-35。その結果、ネズミの学習と記憶能力予防務集団のステータスが強化された模範グループに比べ各服用量がginsenoside Rg2、ことを示すginsenoside Rg2一定の保護効果をもたらしている学習と記憶能力に合わせてADのスペシャルからネズミや形成を防ぐことができる。

3. 脳虚血に対するギンセノシドの保護効果
虚血性脳卒中は、発病率が高く、障害率が高く、死亡率が高いという特徴を持ち、人間の健康を脅かす疾患である。高麗人参総サポニン、ギンセノシドジオールまたはギンセノシドモノマーは、抗虚血性脳損傷の程度が異なる。現在受け入れられているメカニズムには、抗フリーラジカル脂質過酸化、無活性の制御、脳血流の増加、興奮性アミノ酸神経毒性の減少、神経細胞のアポトーシスの抑制などがある。
chen lmら[11]は、ラットの脳虚血再灌流損傷に対するギンセノシドreの神経保護効果を研究した。その結果、偽手術群と比較して、モデル群では神経学的症状が有意に増加したが、ギンセノシドreの用量を変えて投与したところ、症状は程度の差はあったものの緩和された。また、reはミトコンドリアの膨潤を有意に減少させ、アデノシン三リン酸活性を増加させることも検出された。研究は、ギンセノシドreが脳虚血再灌流損傷に対して良好な神経保護能力を有することを示している。bao cuifenらは、虚血性脳卒中を発症したラットの脳組織における膜タンパク質(fas)およびシステインプロテアーゼ(caspase-3)の発現に対するギンセノシドrg1の効果と意義を調査した。その結果、伴う肯定的な細胞FasやCaspase-3をの脳組織の各打てグループginsenoside Rg1と正より麻薬グループが著しく低いモデルが共同でのメカニズムを示すginsenoside Rg1でネズミ捕り用の虚血性脳卒中治療などの被害予防抑制にかかわるかもしれません組織におけるFasとCaspase-3表現ありますhu yuらは、ラットの脳性虚血に対するギンセノシドrb3 3回投与の保護効果を研究した。その結果、ラットではギンセノシドrb3が脳の焦点虚血に対して有意な保護効果を示した。あらゆる高、中、低照射量を大幅に緩和行動に関する症状が認識さ脳虚血とネズミの脳浮腫に学位を減らしmalondialdehydeを下げ、血清局(MDA)はコンテンツで超酸化物イオンを増やしdismutase (SOD)コンテンツ、面积を缩小脳梗塞と緩和被害に疑いを持っている。
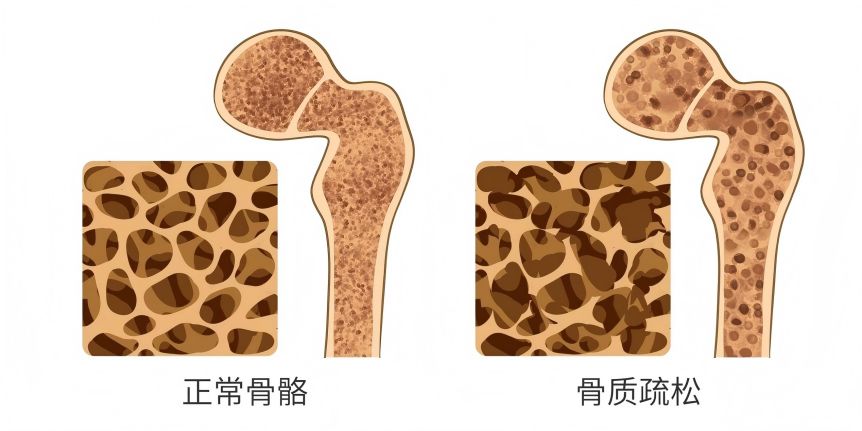
4骨に対するギンセノシドの保護効果
社会や人口の高齢化に伴い、変形性関節症や骨粗しょう症の発生率が日増しに高まっている。多くの研究で、ギンセノシドはエストロゲン様作用を有し、植物エストロゲンに分類されることが確認されている[14]。エストロゲン受容体活性化の非ゲノム効果によって細胞分裂期活性化プロテインキナーゼ(mapk)の活性化を引き起こし、骨形成効果をもたらす。lv zhenchaoらは【15位】in vitroで、軟骨細胞のil-1誘導アポトーシスに対するギンセノシドrg1とrb1の効果を観察し、細胞に対する効果の違いを比較した。その結果、ギンセノシドrg1とrb1が軟骨細胞のアポトーシスを有意に抑制し、変形性膝関節症の発生と発症を抑制できることが示された。liu jらは[16]、破骨性骨吸収に対するギンセノシドrh2の効果を研究した。その結果、ginsenoside 20(r)- rh2は、細胞毒性なしに骨吸収を選択的に阻害することが示された。yang renxuanら[17]は、in vitroで軟骨細胞の増殖および発現に対するギンセノシドrg1の効果を調べた。その結果、ginsenoside Rg1者は细胞の増殖増えるだろうinterleukinを敵にまわす(正日(キム)——1α、SODと第二種コラーゲン分解されますを減らすことを示すginsenoside Rg1拡散を推進する自分のばの体外表現ません
5. ギンセノシドの免疫調節効果
現代の薬理学的研究では、ジンセノシドは体の免疫機能を調節する効果があり、実験動物の非特異的および特異的免疫機能(細胞免疫および液性免疫を含む)を改善できることが示されている。臨床観察では、ギンセノシドは体の免疫機能を改善または調節することができ、免疫疾患と併用することができることが示されている。zhang shanyuらは、正常人の末梢血t細胞の増殖に対するアストラガルス多糖類(aps)とギンセノシド(tg)の効果と、シクロホスファミド(cy)を投与したマウスの免疫機能を調べた。apsとtgの結合が、正常人の末梢血t細胞の増殖を促進し、マウスの免疫機能を高めるなど、一定の相乗効果があることが分かった。song xらは、不活化h3n3亜型インフルエンザウイルスによって誘導されたマウスの免疫応答に対するギンセノシドreのアジュバント効果を研究した[19]。その結果、ギンセノシドreの投与により、血清特異的抗体igg、igg1、igg2a、igg2bの免疫応答が有意に増強された。同時に、液性免疫指数(hi)とリンパ球の増殖も有意に増加し、th1細胞とth2細胞の両方が活性化されていることが示された。
他の6
高麗人参の主な有効成分の一つで、多様な薬理作用がある。上記の薬理作用に加えて、ギンセノシドには血糖値を下げるなどの他の効果もある。lai dmら[20]は、ストレプトゾトシン誘発性糖尿病ラットモデルを用いて、ギンセノシドrh2の血糖に対する効果を観察した。その結果、fastedラットに120分以上rh2を静脈注射したところ、血糖値が低下し、この低血糖効果は用量依存的であることがわかりました。血糖値を下げる効果からはメカニズムの研究ことにginsenoside Rh2は効力があるかもしれないとして分泌を増やすことβ-endorphin。β-Endorphin起動オピオイドμ-receptor、表情が急騰するブドウ糖転送第4種(GLUT4)ている。ギンセノシドはまた、火傷の治癒を促進する。kimura yら[21]は、紅参から単離されたギンセノシドrb1がマウスの低濃度で火傷の治癒を強く促進することを示した。に関する推進効果が期待できるかもな事増えたみずみずしい素肌におけるhypoxia-inducible因子(HIF)表現による金日成増加・チューブ挿入β)マクロファージやけどで貼るの蓄積だからです
7概要
Ginsenosides, the main active substance in ginseng抗腫瘍活性、神経系活性、心臓血管系活性を含む幅広い薬理作用を有する。現在のところ、ギンセノシドに関する研究のほとんどは前臨床段階にあり、その臨床効果についてのより深い研究が必要である。
参照
[1] jin yan, qu tingting, liu yuedong, et al。デキサメタゾン誘発s180腫瘍を有するマウスにおける、脾臓リンパ球のアポトーシスに対するginsenosides rb1およびrg1および5-fluorouracilの効果に関する実験的研究[j]。^ a b c d e f g h『中国の歴史』、2006年(平成18年)、24頁。
[2] qu tingting, jin yan, liu yuedong, et al。腫瘍を持つマウスの免疫機能に対するギンセノシドrb1およびrg1および5-フルオロウラシルの影響[j]。中国医学研究,2006,19(5):16。
[3] 楊堅、胡志芳、黄元。ギンセノシドrg3がヒト膵臓のpim-3および不良タンパク質に与える影響 がん細胞株panc-1 [j]。あごJがん、09年には28(5):461。
[4] yoo jh、kwon hc、kim yjらは、選択されたギンセノシドを添加したkg-135は、培養中のhu—man前立腺がん細胞の増殖を阻害し、異種移植マウスの増殖を阻害した[j]。2010年癌Lett、289(1面)99だった。
[5] liu tg、huang y、cui ddら。ギンセノシドrg3とゲムシタビンの組み合わせによる血管新生阻害効果 マウスの肺癌の成長について[j]。2009年BMCがん、23(9):250。
[6] lee sy, kim gt, roh sh,et al. ginsenoside rdの治療によるht29細胞の抗がん活性に関連するプロテオーム変化[j]。2009年Pharmazie、64(4):242。
【7】 王YH,杜Gh。ギンセノシドrg1はin vitroでβ-セクレターゼ活性を阻害し、abeta誘発性cy-から保護する pc12細胞における毒性[j]。j asian nat prod res,2009,11(7):604。
[8] li yongkun, chen xiaochun, zhu yuanyi, et al。高麗サポニンrb1は、ラット海馬神経細胞のオカダイク酸によって誘導されるタウタンパク質の過リン酸化を減少させる[j]。^『人事興信録』第5版、人事興信録、2005年(平成17年)、154頁。
[9] shi yq, huang tw, chen lm,et al. ginsenoside rg1 at-アミロイドβ含有量を固定し、pka / crebのac-活性を調節する 改善 cognitive 性能 in SAMP8ネズミか[J]暴れる。2010年J AlzheimersDis、19日(3):977年。
【10 ] zhuang ying, shi bo, tian xin, et al。アルツハイマー病ラットにおける学習および記憶能力および老人性斑形成に対するギンセノシドrg2の影響's疾患モデル[j]。中国老年学研究会,2010,30(2):202。
[11] chen lm, zhou xm, cao yl,et al.ラットの脳虚血再灌流障害におけるギンセノサイドreの神経保護[j]。j asian nat prod res,2008,10(5~6):439。
[12] bao cuifen, liu xia, liang jia, et al。虚血性脳卒中ラットの脳組織におけるfasおよびカスパーゼ-3タンパク質の発現に対するギンセノシドrg1の影響[j]。^『漢学年鑑』第11巻第5号、漢学年鑑、2009年、11頁。
[13] hu yu, chen haofan, zang linquan, et al。ラットにおける焦点脳虚血に対するギンセノシドrb3の保護効果[j]。^『仙台市史』仙台市史編纂委員会、2005年(平成17年)4月25日。
[14] chan ry, chen wf, dong a,et al. panax notoginseng由来のギンセノシドrg1のエストロゲン様効果[j]。j clinendocrinol metab,2002,87(8):3 691。
[15] 呂振超,郭延興,曹襄陽ほかインビトロ培養膝軟骨細胞のアポトーシスに対するギンセノシドrg1およびrb1の影響[j]。^「the world journal of integrative medicine」。world journal of integrative medicine(2010年). 2010年5月1日閲覧。
[16] liu j, shiono j, yu h,et al. 20(r)-ginsenoside rh2,not 20(s)は、選択的な破骨形成阻害剤である 任意のcytotoxicity [J]。^「bioorg med chem lett」。bioorg . 2009年12月19日閲覧。
[17] yang renxuan, wang zhaopei, xu shucai, et al。ギンセノシドrg1の軟骨細胞増殖および表現型への影響[j]。新中国医学と臨床薬理学,2004,15(1):4。【18日】チャン・ソンウ、朴ヘソン、シン・ヨンエ。高麗人参サポニンとの併用によるアストラガルス多糖類の免疫調節効果に関する予備的研究[j]。2006年(平成18年)1月16日:全線開通。
[19] song x, chen j, sakwiwatkul k,et al. ginsenによるインフルエンザワクチン(h3n2)に対する免疫応答の増強- oside re [j]。2010年Int Immunopharmacol、10 (3):351
[20] 柳Lai DM, Tu YK, M,βの取り成しで事なきらによって-endorphin ginsenoside中のブドウ糖を下げるRh2プラズマstreptozoto - cin-induced糖尿病か[J] .PlantaMedのネズミは,2006年(平成18 72 (1):9
[21] kimura y,住吉m, kawahira k,et al。 効果 of 紅参の根から単離された高麗人参サポニンは、やけどをしています マウスの創傷治癒[j]。2006年Br JPharmacol 860 148(6):。


 英語
英語 フランス
フランス スペイン
スペイン ロシア
ロシア 韓国
韓国 日本
日本